Новости
На риск ранних болезней сердца больше влияют нездоровый образ жизни и сопутствующие заболевания, чем генетическая предрасположенность.
В работе, представленной на конгрессе Европейского общества кардиологии, исследовалось влияние наследственных и прижизненных факторов на риски ранних заболеваний сердца.
В исследовании приняли участие 1075 человек. Из них у 555 пациентов была диагностирована так называемая преждевременная ишемическая болезнь сердца с анамнезом, включавшим стабильную и нестабильную стенокардию, сердечный приступ, а 520 человек составили контрольную группу. Средний возраст и половой состав: 45 лет, 87% мужчины — в основной группе, 44 года и 86% мужчин — в контрольной. Пациенты и контрольные группы набирались из базы данных Genes in Madeira и Coronary Disease (GENEMACOR). По обеим группам замерялись факторы риска и генетические предрасположенности.
Преждевременная ишемическая болезнь сердца, то есть ранняя (до 55 лет) патология снабжения кровью миокарда, возникает из-за поражения коронарных артерий. Мужчины страдают от этого заболевания чаще женщин, этим обусловлен гендерный состав участников исследования.
У участников исследования замеряли пять модифицируемых факторов риска: частое курение, отсутствие физической активности, диабет, повышенный уровень холестерина, высокое давление. Также всем участникам провели секвенирование генома, чтобы оценить риски ишемической болезни сердца или, например, повышенного давления, которые могут быть связаны с наследственностью.
Семьдесят три процента пациентов имели как минимум три фактора риска из пяти. При этом в контрольной группе три фактора и более имели всего тридцать один процент людей. Кроме того, факторы оказались прочно связаны с ишемической болезнью сердца: в обеих группах вероятность ее возникновения росла экспоненциально с каждым новым фактором риска. Вероятность развития заболевания была в три раза выше при наличии одного фактора, в семь раз выше — при наличии двух, а в 24 раза выше — при наличии трех.
Генетическая оценка риска, содержащая 33 варианта, которые, как предполагается, способствуют развитию ишемической болезни сердца, а также предрасположенности к другим факторам, показывает, что средний балл у пациентов — по сравнению с контрольной группой — выше. Однако, по результатам работы, вклад генетики в риск возникновения и развития ишемической болезни сердца снизился, так как выросло количество модифицируемых факторов.
Автор исследования, доктор Жоао А. Соуза из больницы Фуншала, Португалия, отмечает: «В своей клинической практике мы часто слышим, как молодые пациенты с преждевременными сердечными заболеваниями «ищут убежища» и объяснений в своей генетике/семейной истории. Однако, если посмотреть на данные нашего исследования, эти молодые пациенты часто бывают курильщиками, физически неактивными, с высоким уровнем холестерина и высоким кровяным давлением — и все это можно изменить».
Как указывают авторы, несмотря на то, что данные подтверждают влияние генетики на развитие ишемической болезни сердца, внешние факторы влияют намного сильнее. И чем больше внешних факторов, тем меньшую роль играет собственно генетическая предрасположенность. При этом именно пациенты с такой предрасположенностью должны быть внимательнее к тому, чтобы вести здоровый образ жизни.
«Наше исследование предоставляет убедительные доказательства того, что люди с семейной историей преждевременных пороков сердца должны вести здоровый образ жизни, поскольку их плохое поведение может быть более серьезным фактором, способствующим развитию сердечных заболеваний, чем генетика. Это означает, что нужно бросить курить, регулярно заниматься спортом, соблюдать здоровую диету, а также проверять артериальное давление и уровень холестерина», — подытоживает Соуза.
В День знаний, 2 сентября, возобновил после летних каникул свою деятельность учебно-тренировочный отдел Центра.
Первое занятие, которое провели инструкторы-преподаватели школы медицины катастроф, было выездным, и прошло оно в детском учреждении санаторного типа "Незабудка" для детей, которые находятся в нём на оздоровлении.

Ребятам рассказали о работе скорой помощи и правилах обращения в службы экстренного реагирования. Они узнали, как, в случае необходимости, самим осуществить вызов, какие правила следует при этом соблюдать и как отвечать на вопросы диспетчера.
Не осталось без внимания оказание первой доврачебной помощи, о которой ребята узнали в доступной форме. Им наглядно продемонстрировали, как необходимо фиксировать конечности при переломах, накладывать жгут при кровотечениях; кроме того, рассказали, какие подручные средства можно использовать, оказывая помощь. При этом в качестве статистов выступали и дети, и воспитатели. Также детворе показали манекены, на которых в учебных классах Центра проводят обучение и отрабатывают приёмы по оказанию первой помощи.

Интерес вызвало знакомство с автомобилем скорой помощи – его оснащением и используемой аппаратурой. Детей обрадовала возможность побывать внутри салона, увидеть всё, потрогать своими руками и сделать фото на память. С интересом они воспринимали для себя всё новое. Звуки сирены и подмигивание проблесковых маячков завершили встречу.
Неалкогольная жировая дистрофия печени была впервые описана как отдельная клиническая единица четыре десятилетия назад. Тем не менее, она стала центром внимания гепатологов из-за высокой распространенности и возрастающего влияния на прогрессирование болезни печени до терминальной стадии. В связи с этим, в данной статье предлагается к прочтению обзор информации.
Неалкогольная жировая дистрофия печени (НАЖДП) вызвана накоплением жира в печени; состояние может прогрессировать с течением времени, увеличивая риск развития цирроза и гепатоцеллюлярной карциномы. Распространенность быстро растет из-за глобального распространения ожирения и сахарного диабета 2 тип; по расчетам ученых НАЖДП станет показанием номер 1 для трансплантации печени в течение следующего десятилетия.
.
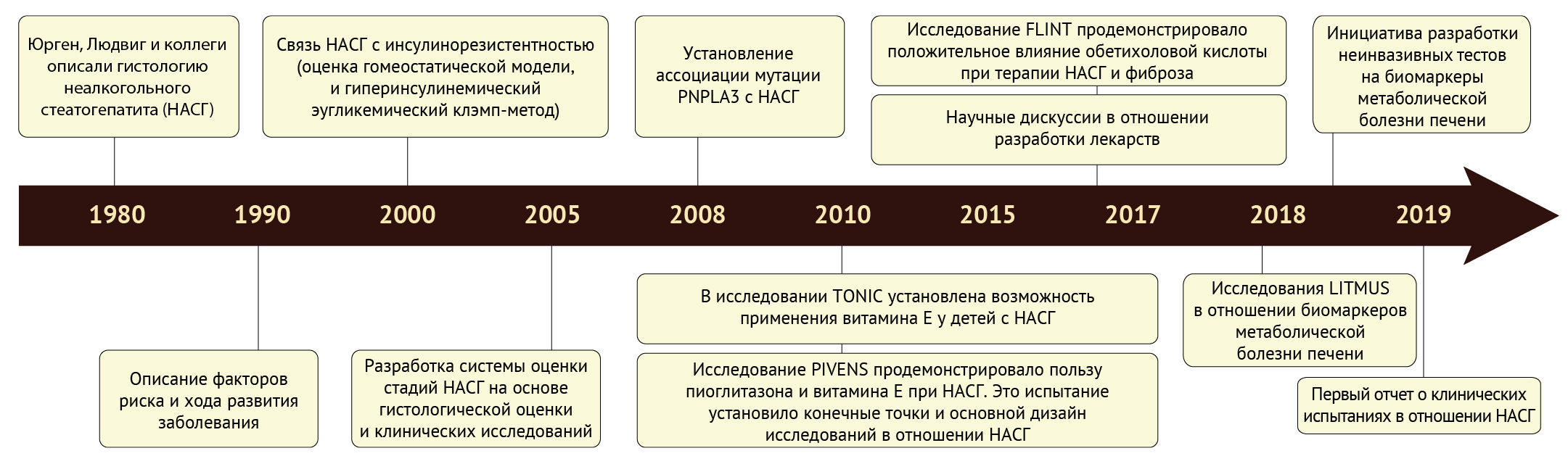
Рисунок 1. Хронология основных событий в мире науке, связанных с неалкогольной жировой дистрофией печени
Уже сейчас неалкогольная жировая болезнь печени является самой распространенной хронической болезнью печени во всем мире. Ученые оценили распространенность, частоту и результаты НАЖДП среди населения Азии, проведя анализ исследований, в которых сообщалось о распространенности, заболеваемости и исходе НАЖДП в PubMed, EMBASE и Кокрановской библиотеке с момента создания ее базы данных до 17 января 2019 года. Были учтены только те исследования, которые охватывали разные группы людей и многолетние обсервационные исследования пациентов с НАЖДП, диагностированной по УЗИ, показателям сыворотки крови или биопсии печени. Двое ученых независимо друг от друга проверяли и анализировали данные. Суммарные оценки были рассчитаны с использованием модели со случайными эффектами. Исследование зарегистрировано в PROSPERO, номер CRD42018088468.
Для анализа были отобраны 237 исследований (13 044 518 участников). Общая распространенность НАЖДП, независимо от метода диагностики, составила 29,62 %. Распространенность НАЖДП значительно увеличивалась с течением времени (25–28 % в период с 1999 по 2005 год, 28,46 % в период с 2006 по 2011 год и 33,90 % между 2012 и 2017). Суммарный годовой уровень заболеваемости НАЖДП составил 50,9 случая на 1000 человеко-лет. У пациентов с НАЖДП ежегодная заболеваемость гепатоцеллюлярной карциномой составила 1,8 случаев на 1000 человеко-лет , а общая смертность — 5,3 на 1000 человеко-лет. Распространенность НАЖДП в мире и особенно в Азии растет и связана с плохими исходами, включая гепатоцеллюлярную карциному и смерть.
Также становится все более очевидным, что НАЖДП не только влияет на печень, но также может увеличить риск развития других заболеваний, включая СД 2 типа, сердечно-сосудистые заболевания и хронические заболевания почек (ХБП), которые являются распространенной проблемой здравоохранения. Накопленные данные свидетельствуют о том, что НАЖДП усиливает резистентность к инсулину, предрасполагает к атерогенной дислипидемии и способствует высвобождению различных провоспалительных факторов, протромботических факторов и профиброгенных молекул, которые могут способствовать повреждению тканей сосудов и почек. Кроме того, взаимовлияние пораженных органов или тканей друг на друга при этих заболеваниях может привести к дальнейшему нарушению функции и ухудшению прогнозов лечения. Все больше фактических данных указывает на тесную связь между НАЖДП и ХБП. Существуют причинно-следственные связи между НАЖДП и ХБП или нет — еще предстоит установить окончательно.
Клиника
НАЖДП — это термин, который охватывает весь клинико-патологический спектр заболеваний печени, начиная от простой жировой инфильтрации более 5 % гепатоцитов (простой стеатоз печени), до жировой инфильтрации, совмещенной с воспалением (неалкогольный стеатогепатит; НАСГ) до прогрессирующего фиброза и, в конечном счете — цирроза, который может прогрессировать до гепатоцеллюлярной карциномы.
Диагноз НАЖДП основан на трех критериях:
- стеатоз печени, подтвержденный на УЗИ или гистологически;
- умеренное потребление алкоголя — обычно 20 г в день для женщин и 30 г в день для мужчин;
- отсутствие конкурирующих причин для стеатоза печени (таких как вирусы, лекарства, избыток железа или аутоиммунитет).
В целом, клинические признаки и симптомы заболевания печени отсутствуют у большинства пациентов с НАЖДП на момент постановки диагноза; умеренная гепатомегалия часто является единственным признаком, хотя некоторые пациенты сообщают об усталости и чувстве сытости или дискомфорта в животе. У значительного числа пациентов с НАЖДП наблюдаются типичные признаки метаболического синдрома (абдоминальное ожирение, атерогенная дислипидемия, гипертония, резистентность к инсулину, непереносимость глюкозы или сахарный диабет 2 типа).
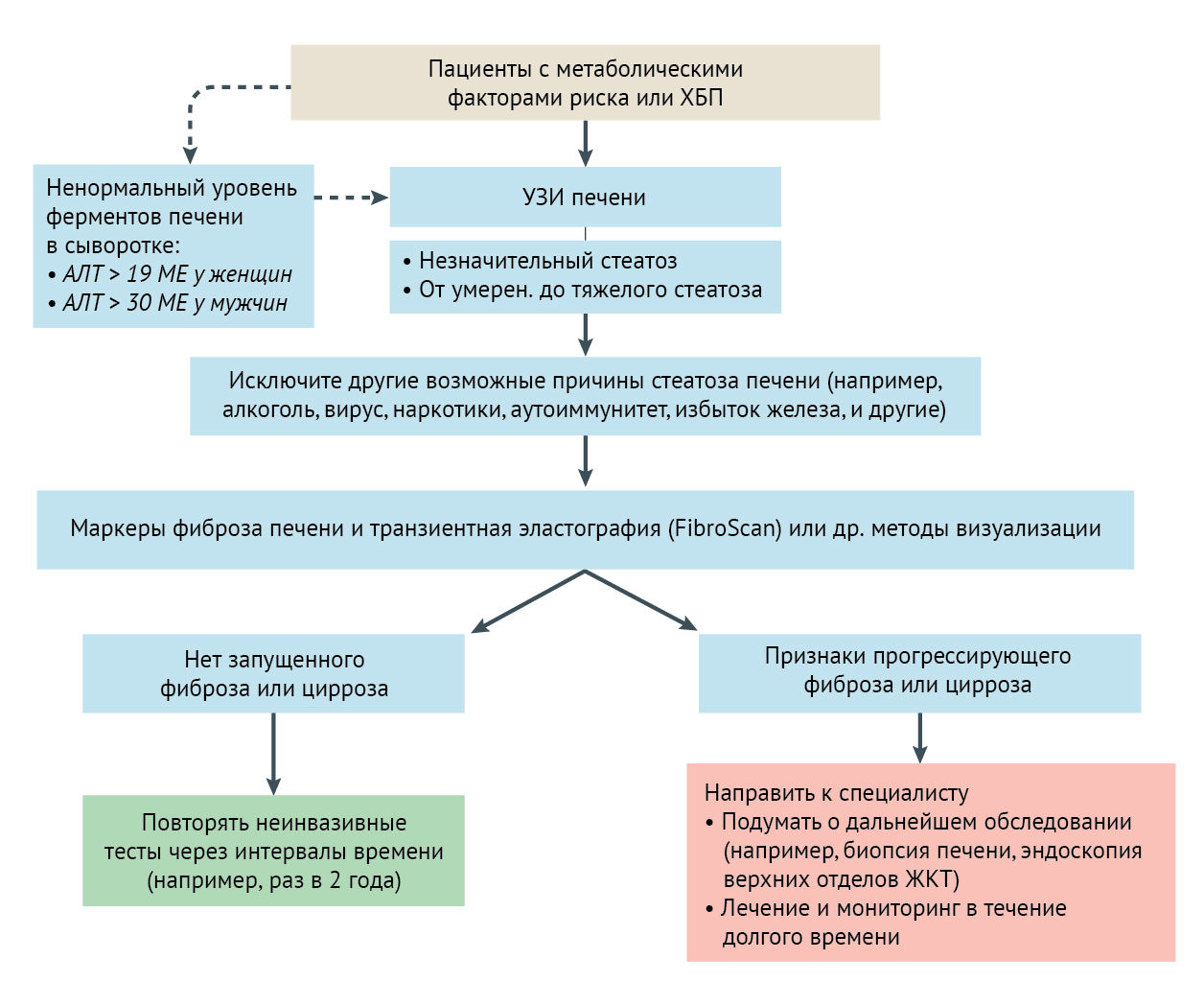
Наиболее распространенной и часто единственной патологией, обнаруживаемой при лабораторных исследованиях у пациентов с НАЖДП, является умеренно повышенный уровень ферментов печени в сыворотке (аминотрансферазы и γ-глутамилтрансферазы). Другие нарушения (например, тромбоцитопения, повышение уровня билирубина и увеличение протромбинового индекса) могут быть обнаружены у пациентов с более запущенной дистрофией (например, цирроз). Однако уровень ферментов печени в сыворотке не является надежными маркером для скрининга и диагностики НАЖДП и поэтому не должен интерпретироваться без дальнейшего исследования. У пациентов с нормальными уровнями ферментов печени в сыворотке крови вполне может быть диагностирована НАЖДП.
УЗИ печени является рекомендуемым методом визуализации первой линии для выявления НАЖДП в клинической практике. При ультразвуковом исследовании стеатоз печени характеризуется типичным диффузным увеличением эхогенности (так называемая светлая печень). Ультрасонография выявляет стеатоз печени с хорошей диагностической точностью, демонстрируя чувствительность и специфичность приблизительно 85 % и 95 %, соответственно (при инфильтрации печени жиром не менее 20-30 %). Кроме того, ультрасонография относительно недорога и может помочь клиницистам исключить другие причины заболеваний печени и выявить любые ранние признаки цирроза или портальной гипертензии. На сегодняшний день Т1-взвешенная МРТ с двойным эхом и протонная магнитно-резонансная спектроскопия определяют стеатоз печени с наилучшей диагностической точностью. Протонная магнитно-резонансная спектроскопия позволяет количественно оценить содержание триглицеридов в печени, обладает превосходной воспроизводимостью и чувствительностью, но требует значительных ресурсов и не может надежно отличить простой стеатоз от неалкогольного стеатогепатита.
Прогрессирование от простого стеатоза до НАСГ и далее до прогрессирующего фиброза, а также масштаб и стадия фиброза представляют особый клинический интерес, поскольку известно, что осложнения, связанные с терминальной стадией заболевания печени, возникают у пациентов с НАЖДП, у которых диагностирован прогрессирующий фиброз. Биопсия печени остается стандартной процедурой диагностики НАСГ и установления степени поражения печени и фиброза у пациентов с более запущенной НАЖДП, но эта процедура является инвазивной, потенциально рискованной и может привести к ошибочному результату, поэтому она не подходит для мониторинга пациентов или для диагностики в больших группах. Ряд неинвазивных тестов на биомаркеры, большинство из которых требуют дальнейшей проверки могут быть полезны для выявления пациентов с НАЖДП, которым требуется биопсия печени для постановки окончательного диагноза. Чувствительность и специфичность этих неинвазивных тестов для оценки прогрессирующего фиброза печени также были описаны.
Система оценки фиброза FIB-4 score учитывает клинические и лабораторные переменные, такие как: возраст, уровень аминотрансфераз и альбумина в сыворотке, количество тромбоцитов, индекс массы тела и статус диабета. Расширенный тест фиброза печени (ELF) и FibroTest являются примерами запатентованных методов, которые были предложены для неинвазивной оценки прогрессирующего фиброза печени в соответствии с конкретными сывороточными биомаркерами. Другой подход к постановке диагноза фиброза печени, известный как FibroScan, измеряет скорость низкочастотной упругой волны, распространяющейся через печень: чем жестче ткань, тем быстрее распространяется волна. Тем не менее, во многих случаях (~ 20 % пациентов; в основном, пациенты с ожирением), этот подход не гарантирует точного результата, и его использование нежелательно у пациентов с ожирением.
.
.
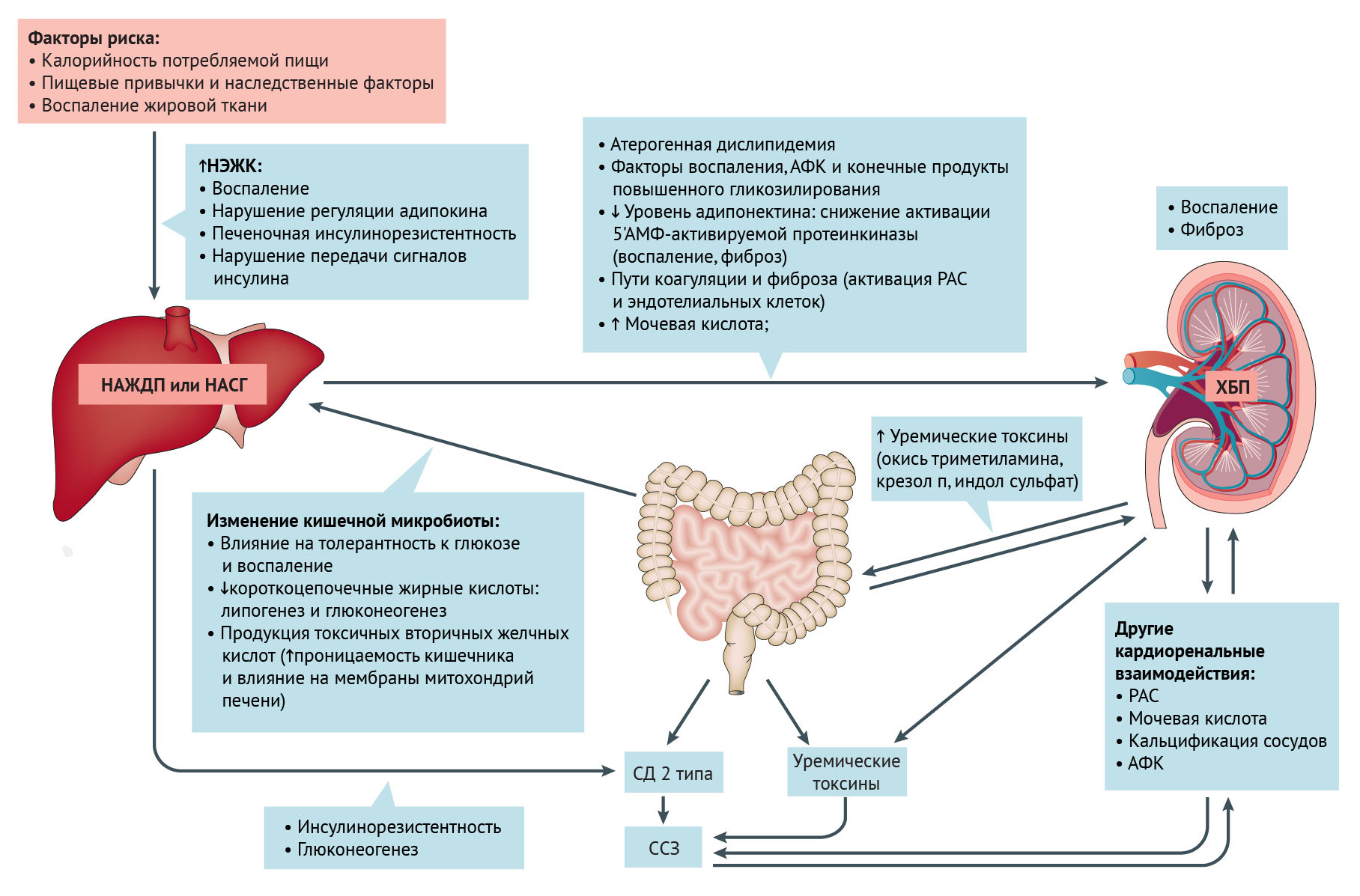
Прогрессирование дисфункции печени запускает пути, которые могут влиять на развитие ХБП. Например, инсулинорезистентность и атерогенная дислипидемия, а также провоспалительные факторы, протромботические факторы и профиброгенные молекулы могут способствовать повреждению тканей сосудов и почек. Снижение активации 5ʹ-AMP-активированной протеинкиназы в ответ на снижение уровня адипонектина дополнительно стимулирует провоспалительные и профиброгенные механизмы. Активация ренин-ангиотензиновой системы и эндотелиальных клеток также может способствовать дисфункции печени и почек за счет усиления окислительного стресса, воспаления и процессов коагуляции.
Повышенная продукция уремических токсинов кишечной микробиотой в условиях ХБП может вызывать дальнейшее повреждение почек, печени и сердечно-сосудистой системы через воспалительные, окислительные и фиброзные пути. Дисбиоз кишечной микробиоты, который часто возникает при ожирении, потенциально влияет на НАЖДП, ХБП и сахарный диабет 2 типа через сложные механизмы. Наконец, сердечно-сосудистые заболевания (ССЗ), риск которых увеличивается при НАЖДП, СД 2 типа или дисбиозе кишечника, могут влиять на развитие почечной дисфункции (и наоборот) посредством кардиоренальных взаимодействий.
Неалкогольная жировая дистрофия печени (НАЖДП) тесно связана с печеночной инсулинорезистентностью. Накопление печеночного диацилглицерина активирует PKC-ε, нарушая активацию рецептора инсулина и стимулированный инсулином синтез гликогена. Резистентность периферического инсулина косвенно влияет на метаболизм глюкозы и липидов в печени, увеличивая поток субстратов, которые способствуют липогенезу (глюкоза и жирные кислоты) и глюконеогенезу (ацетил-КоА, происходящий из глицерина и жирных кислот, аллостерического активатора пируваткарбоксилазы). Потеря веса с помощью диеты или бариатрической хирургии эффективно лечит НАЖДП, но лекарства, специально одобренные для лечения НАЖДП, отсутствуют. Некоторые новые фармакологические препараты широко применяются для изменения энергетического баланса или влияния на пути, которые способствуют НАЖДП (например, агонисты для PPAR γ, PPAR α / δ, FXR и аналоги для FGF-21 и GLP-1). Другие специфически ингибируют ключевые ферменты, участвующие в синтезе липидов (например, митохондриальный переносчик пирувата, ацетил-КоА-карбоксилаза, стеароил-КоА-десатураза и моноацил- и диацил-глицерол-трансферазы). Наконец, новый класс митохондриальных разобщающих агентов, нацеленных на печень, увеличивает расход энергии на гепатоцеллюлярные клетки, препятствуя метаболическим и печеночным осложнениям НАЖДП.
Министерство здравоохранения ЛНР в ближайшее время планирует закупить для лечебных учреждений Республики машины скорой помощи и медицинское оборудование. Об этом на брифинге в ЛуганскИнформЦентре сообщила министр здравоохранения ЛНР Наталья Пащенко.
Она отметила, что на сегодняшний день ведомство ведет работу по оптимизации системы здравоохранения, что позволит повысить качество медицинских услуг и улучшить условия оказания помощи.
"На сегодняшний момент уже ведется работа над приведением в соответствие коечного фонда, и уже в ближайшее время мы планируем начать глобальные перемены в здравоохранении по модернизации именно системы и по улучшению качества оснащения нашего здравоохранения", - сказала министр.
"Будут в этом году, я думаю, закуплены машины скорой медицинской помощи. Это первый глобальный шаг по улучшению оказания экстренной неотложной помощи. Планируется также закупка оборудования в ближайшее время, так как материально-техническая база крайне устаревшая", - сообщила Пащенко.
Руководитель Минздрава уточнила, что оборудование в медучреждениях Республики не обновлялось более 60 лет.
"Пока что первые шаги сделаны по оснащению наших республиканских учреждений, таких как республиканская клиническая больница, республиканская детская клиническая больница, онкологический диспансер", - добавила она, отметив, что теперь внимание Минздрава сосредоточено на обеспечении первичного звена.
"То есть, поликлиники и стационары сегодня должны получить аппаратуру, диагностическую, лечебную. Та, которая позволит своевременно и качественно установить диагноз и приступить к своевременному, качественному, полному лечению, и принесет пациенту скорейшее выздоровление", - рассказала Пащенко.
Ранее глава ЛНР Леонид Пасечник провел в Луганске совещание с главами городов и районов Республики, а также представителями министерств ЛНР по вопросу оптимизации системы здравоохранения.
Пащенко также сообщала, что Министерство здравоохранения ЛНР с целью повышения уровня оказания помощи населению пересматривает направления финансирования в отрасли.
ЛуганскИнформЦентр — 30 августа — Луганск
Министерство здравоохранения ЛНР ведет работу по реорганизации луганской Специализированной железнодорожной больницы в Клинику медицины катастроф. Об этом на брифинге в ЛуганскИнформЦентре сообщила министр здравоохранения ЛНР Наталья Пащенко.
Ранее Правительство ЛНР приняло распоряжение о реорганизации железнодорожной больницы путем присоединения учреждения к Луганскому республиканскому центру экстренной медицинской помощи и медицины катастроф. Итогом процедуры станет создание Клиники медицины катастроф как филиала Центра. Завершить реорганизацию планируется до 31 марта 2020 года.
"Еще один глобальный и важный шаг сделан сегодня Министерством здравоохранения – уже идет работа над пересмотром функций нашей железнодорожной больницы, которая ранее обслуживала только спецконтингент. Сегодня эта больница будет участвовать в оказании помощи всему населению как Луганска, так и наших регионов", - отметила Пащенко.
"Это будет клиника катастроф, в которой мы уже открываем сейчас деятельность военно-врачебной комиссии совместно с Народной милицией и при поддержке Правительства", - уточнила министр.
Она добавила, что такой вопрос "назрел очень давно, он важен для Республики и очень глобален".
ЛуганскИнформЦентр — 30 августа — Луганск
Бронхиальная астма (БА) — это гетерогенное заболевание, характеризующееся наличием хронического воспаления дыхательных путей и респираторных симптомов (сухие хрипы, одышка, стеснение в груди и кашель), интенсивность которых изменяется с течением времени, а также вариабельностью в отношении ограничения экспираторного потока.
Симптомы астмы могут купироваться как самостоятельно, так и с помощью медикаментов. Проявления БА зачастую усугубляются ночью или ранним утром, а также провоцируются вирусной инфекцией (простуда), физической нагрузкой, аллергенами, изменениями погоды, смехом, ирритантами (выхлопные газы автомобилей, дым и сильные запахи) и другими факторами.
Снижают вероятность диагноза изолированный кашель без других респираторных симптомов, хроническая продукция мокроты, одышка, сопровождающаяся головокружением, предобморочным состоянием или периферическими парестезиями (чувство покалывания, жжения в дистальных отделах конечностей), боль за грудиной, а также инспираторная одышка, обусловленная физической нагрузкой.
Фенотипы астмы
Как говорилось выше, бронхиальная астма — гетерогенное заболевание с различным течением процесса. Демографический кластер, клинические и/или патологические характеристики заболевания называются «фенотипом астмы». Наиболее часто встречаемые «фенотипы астмы»:
Аллергическая
Самый распространенный фенотип астмы. Часто выявляется в детстве, обычно характерно наличие обширного семейного и/или личного аллергологического анамнеза (экзема, аллергический ринит, пищевая или лекарственная аллергия и т. д.). При исследовании мокроты пациентов часто выявляется воспаление дыхательных путей с эозинофильной инфильтрацией. Пациенты с данным фенотипом хорошо отвечают на терапию ингаляционными глюкокортикостероидами (ИГКС).
Неаллергическая
Выделяется у взрослых пациентов при отсутствии аллергии в анамнезе. Клеточный профиль их мокроты может быть нейтрофильным, эозинофильным или содержать лишь незначительное количество воспалительных клеток. Пациенты данной группы зачастую хуже отвечают на терапию ИГКС.
Астма с поздним началом
Чаще выявляется у женщин, первые проявления возникают во взрослой жизни. В большинстве случаев это пациенты без аллергии, требующие высоких доз ИГКС или относительно невосприимчивые к лечению глюкокортикостероидами.
Астма с фиксированным ограничением экспираторного потока
У части пациентов с длительным течением астмы ограничения экспираторного потока становятся необратимыми из-за ремоделирования стенок дыхательных путей.
Астма с ожирением
В эту группу, собственно, входят пациенты с ожирением и респираторными проявлениями астмы, а также незначительной эозинофилией мокроты.
Перекрест бронхиальной астмы и ХОБЛ (ПБАХ)
Перекрест бронхиальной астмы и ХОБЛ (ПБАХ) характеризуется персистирующим ограничением экспираторного потока c проявлениями, всегда ассоциирующимися с астмой (молодой возраст, значительная вариабельность ограничения экспираторного потока, положительный тест с бронходилататором), а также c некоторыми проявлениями, всегда ассоциирующимися с ХОБЛ (возраст старше 40 лет, отсутствие вариабельности потока, снижение емкости легких, отсутствие ответа на бронходилататор).
У некоторых больных, особенно пожилых и курильщиков, сложно провести дифференциальный диагноз астмы и хронической обструктивной болезни легких. Прогноз у таких пациентов значительно хуже, чем у имеющих изолированную БА либо ХОБЛ, и информации о подборе оптимальной терапии для них пока недостаточно. Вот некоторые рекомендации по начальной терапии «сомнительных» пациентов:
- Для пациентов с преобладающими признаками бронхиальной астмы — назначение адекватной контролирующей терапии, включающей ИГКС, при необходимости — добавление длительно действующего бета-2-агониста (ДДБА) и/или длительно действующего антагониста мускариновых рецепторов, но не монотерапия длительно-действующим бронходилататором;
- Для пациентов с преобладающими признаками ХОБЛ — назначение симптоматической терапии с бронходилататором или комбинации ИГКС/бронходилататор (ДДБА и/или длительно действующий антагонист мускариновых рецепторов), но не использовать монотерапию ИГКС;
- Для пациентов с ПБАХ, которых сложно отнести к тому или иному типу — лечение следует начинать с низких или средних доз ИГКС (в зависимости от выраженности симптомов), к лечению добавляется ДДБА и/или длительно-действующий антагонист мускариновых рецепторов. Не применяется монотерапия ДДБА.
Всем пациентам требуется изменение образа жизни (отказ от курения, умеренная физическая активность), а также лечение коморбидной патологии.
Наличие типичных респираторных симптомов бронхиальной астмы, а также характерного анамнеза, является показанием к выполнению спирометрии либо пикфлоуметрии (измерение пиковой скорости выдоха, ПСВ) с целью выявления ограничений экспираторного потока. При тяжелом состоянии пациента и низкой вероятности других диагнозов начинают проведение эмпирической терапии БА ингаляционными глюкокортикостероидами (ИГКС) и короткодействующими бета-2-агонистами (КДБА), и в дальнейшем после оценки состояния больного и эффекта от терапии проводят необходимые диагностические мероприятия для уточнения и подтверждения диагноза.
Проводится ряд тестов, позволяющих оценить степень и обратимость бронхиальной обструкции: оценка увеличения функции легких после введения бронходилататора или после проведенной терапии, снижения функции легких после физической нагрузки или при проведении провокационных тестов с гистамином или метахолином, выявление нарушений функции легких и вариаций потока в течение 1–2 недель при плановых посещениях либо самостоятельно.
Подтипы БА
«Трудно поддающаяся лечению» БА — термин, применяемый для обозначения случаев, когда невозможно достичь контроля БА несмотря на оптимально подобранную терапию. Зачастую это происходит при наличии у пациента отягчающих факторов, таких как наличие коморбидной патологии, низкая приверженность к лечению, присутствие в среде обитания человека неустранимых аллергенов.
Термины «резистентная» или «рефрактерная к лечению астма» применяются для пациентов, у которых течение, обострения и выраженность симптомов БА плохо контролируются, несмотря на высокие дозы ИГКС в сочетании с вторым препаратом контроля (длительно действующие бета-2-агонисты (ДДБА) и/или системные ГКС) и лечение сопутствующей патологии, либо для тех пациентов, у которых теряется контроль при снижении ступени терапии.
Понятие «тяжелая астма» объединяет пациентов с рефрактерной к терапии БА и нелеченной коморбидной патологией.
В рекомендациях GINA последних лет термин «астматический статус» не встречается, плановая и неотложная терапия БА проводится в зависимости от степени тяжести обострения, определяемой по клиническим и инструментальным данным.
Обострение астмы
Обострением БА считается любое выраженное ухудшение симптомов и/или функции легких (снижение ПСВ или ОФВ1) пациента по сравнению с его обычным статусом. Важно, чтобы пациент следил за своим состоянием и отмечал происходящие изменения. Существует необходимость в плане («asthma action plan») лечения и действий при БА, в котором будет четко прописано, что, когда и в каких дозах принимать пациенту с целью самостоятельного купирования приступа БА.
Перед началом лечения обострения бронхиальной астмы (БА) любой степени тяжести необходимо оценить факторы, увеличивающие риск развития связанной с астмой смерти:
- Наличие в анамнезе смертельно опасного обострения астмы с последующим проведением интубации и ИВЛ;
- Госпитализация в стационар или ОАиР по поводу обострения в течение предыдущего года;
- Использование в настоящий момент или недавнее прекращение приема оральных глюкокортикостероидов (ОГКС) как показатель тяжести состояния;
- Отсутствие приема ингаляционных глюкокортикостероидов (ИГКС) в данный момент;
- Чрезмерное использование короткодействующих агонистов бета-2-адренорецепторов (КАБА) — более одной емкости сальбутамола или его эквивалента в месяц;
- Психосоциальные проблемы или психическое заболевание в анамнезе;
- Плохая приверженность к приему медицинских препаратов и/или несоблюдение (отсутствие) плана лечения;
- Пищевая аллергия.

Самопомощь по «asthma action plan» при обострении астмы
Врач, занимающийся лечением БА, должен составить четкий план действий пациента при развитии обострения и обучить его им. Пациент, в свою очередь, должен самостоятельно осуществлять мониторинг функции легких и проходить регулярные осмотры у специалистов.
Изменения в приеме медикаментов, приведенные ниже, осуществляются при развитии обострения в течение 1–2 недель.
— В начале обострения проводится попытка его купирования увеличением дозы обычных препаратов, облегчающих течение астмы (реливеры):
- увеличение частоты использования КДБА (спейсер, ингалятор);
- увеличение частоты использования низких дозы ИГКС/формотерола (максимально 72 мкг/день формотерола);
— При неэффективности этих действий необходимо увеличение дозы препаратов контроля:
- продолжить прием поддерживающей дозы ИГКС/формотерола, увеличить дозу реливера будесонида или беклометазона/формотерола;
- удвоить дозу ИГКС, обдумать возможность увеличения ИГКС до максимальной дозы (максимально 2000 мкг/день в беклометазона дипропионате или его эквивалентах) + КДБА в качестве реливера;
- увеличить в 4 раза дозу ИГКС/формотерола (максимально 72 мкг/день формотерола) + КДБА как реливер;
- перейти на следующую ступень дозировок ИГКС/другого длительно действующего бета-2-агониста (ДДБА) или добавить дополнительный ингалятор ИГКС (до максимальной дозы 2000 мкг/день в беклометазона дипропионате или его эквивалентах) + КДБА как реливер;
— При ухудшении симптомов и неэффективности лечения необходимо добавление оральных глюкокортикостероидов и срочный визит к врачу. Дозировка преднизолона: для взрослых 1 мг/кг/день (максимально 50 мг) в течение 5–7 дней, для детей 1–2 мг/кг/день (максимально 40 мг) в течение 3–5 дней.
Особенности течения обострений у детей
Незамедлительная госпитализация показана, если у ребенка с БА в возрасте 5 лет и младше наблюдаются любые из следующих симптомов:
- При начальной или последующей оценке: ребенок не может разговаривать или пить, цианоз, втяжение межреберных промежутков, сатурация < 92 % при дыхании атмосферным воздухом, отсутствие дыхательных шумов при аускультации;
- Отсутствие ответа на начальную терапию бронхолитиками: отсутствие ответа на 6 ингаляций КДБА (2 отдельные ингаляции, повторяются по 3 раза) в течение 1–2 ч, стойкое тахипноэ (нормальная частота дыхания: < 60 в 1 мин у детей от 0 до 2 мес; < 50 в 1 мин у детей от 2 до 12 мес; < 40 в 1 мин у детей от 1 до 5 лет), несмотря на три ингаляции КДБА, даже если у ребенка наблюдаются клинические признаки улучшения;
- Социальная среда, не позволяющая проводить лечение обострения БА, или неспособность родителя/опекуна осуществлять лечение обострения БА в домашних условиях.
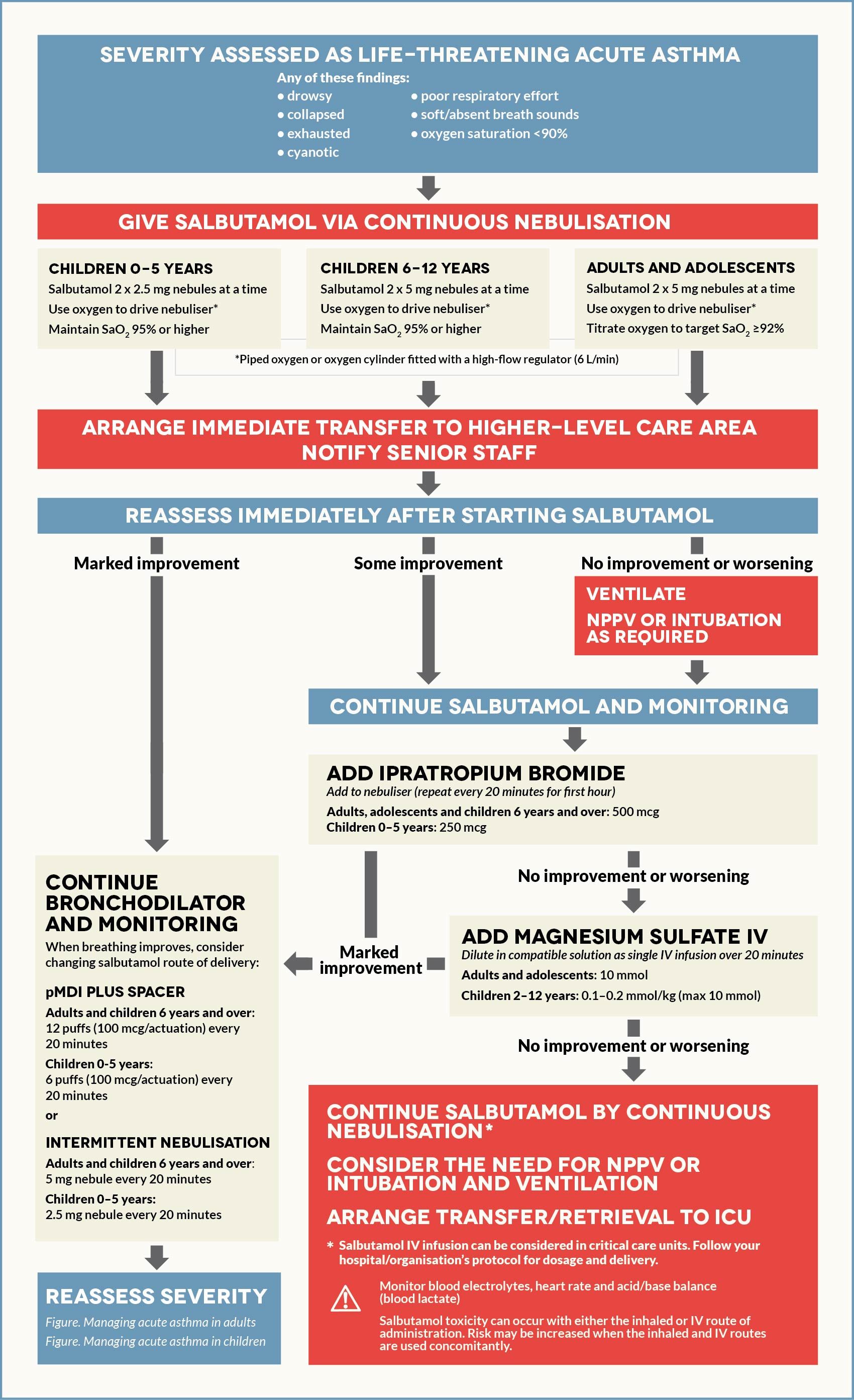
Оказание первой помощи
При поступлении в приемное отделение пациента с обострением астмы необходимо собрать краткий анамнез, провести быстрый осмотр пациента и в максимально ранние сроки начать терапию.
Анамнез
При сборе анамнеза важно учесть несколько моментов:
- время начала и причину (если известно) текущего обострения;
- тяжесть симптомов астмы, включая ограничение физической нагрузки и нарушения сна;
- наличие симптомов анафилаксии;факторы риска связанной с астмой смерти (см. выше);
- наименования медикаментов (для контроля и облегчения симптомов), дозировки и их изменения, устройства для введения данных препаратов и ответ на назначенную терапию, приверженность к лечению.
Степени тяжести
Степень тяжести течения БА у пациента может определяться с помощью физикального обследования (определение возможного угнетения сознания, оценка поведения и речи, частота пульса, дыхания, участие дополнительных мышц в акте дыхания, артериальное давление, сухие хрипы в легких при аускультации и на расстоянии) и объективных методов (пульсоксиметрия, пикфлоуметрия). Сатурация < 90 % как у детей, так и у взрослых служит грозным симптомом и требует агрессивной терапии. Необходимо выявление усугубляющих сопутствующих факторов, таких как анафилаксия, пневмония, пневмоторакс, а также учитывать возможность развития одышки в результате других состояний и заболеваний (сердечная недостаточность, обструкция инородным телом, легочная эмболия, дисфункция верхних дыхательных путей).
Лечение
Главной целью терапии БА является быстрое устранение обструкции дыхательных путей и гипоксемии, для чего проводится назначение короткодействующих бронходилататоров, раннее применение системных кортикостероидов и контролируемая подача кислорода.
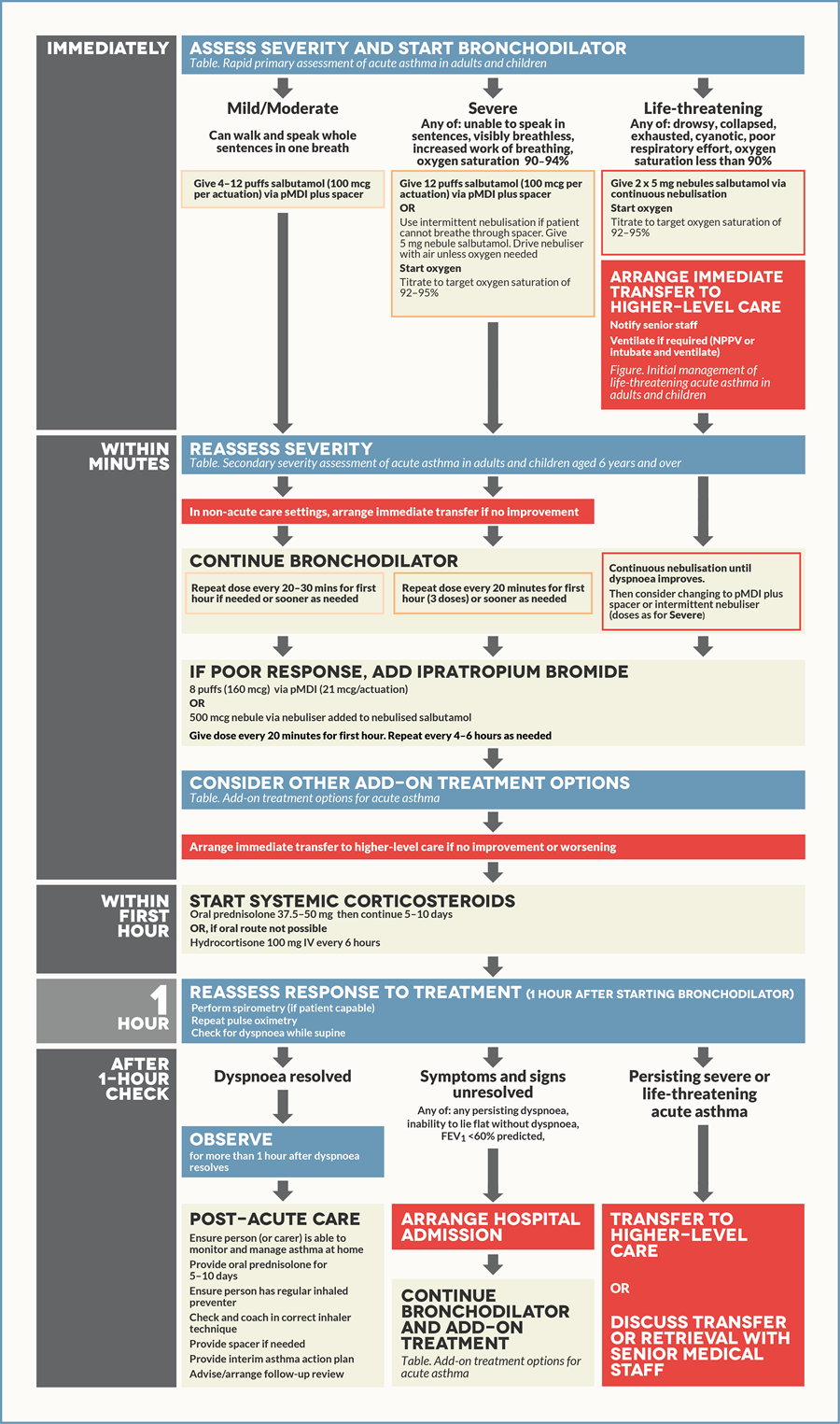
Ингаляция короткодействующих агонистов бета-2-адренорецепторов
Одним из самых эффективных способов устранения обструкции воздухоносных путей является ингаляция КДБА. Для купирования приступа астмы допустимо применение ингаляторов (дозированный аэрозольный ингалятор (pDMI) со спейсером или порошковый ингалятор (DPI)), однако зачастую при их использовании пациенты допускают ошибки, что приводит к снижению эффективности терапии. При невозможности использовать ингалятор применяют небулайзер.
Для обострений легкой и средней степеней тяжести применяют повторные ингаляции КДБА (до 4–10 вдохов каждые 20 минут в течение первого часа). После первого часа доза КДБА варьирует от 4–10 вдохов каждые 3–4 часа до 6–10 вдохов каждые 1–2 часа и более. Примерное содержание лекарственных средств в 1 дозе ингалятора: сальбутамол — 100 мкг, тербуталина сульфат — 250 мкг, фенотерола гидробромид — 200 мкг, левалбутерол — 45 мкг. Дополнительные ингаляции КДБА не требуются, если имеется хороший ответ на начальную терапию (пиковая скорость выдоха (ПСВ) > 60–80 % от должной или личного максимального результата за 3–4 часа).
Кислородотерапия
Кислородотерапию необходимо проводить под контролем сатурации смешанной крови: целевым является ее уровень 93–95 % для взрослых и 94–98 % для детей 6–11 лет. При отсутствии возможности измерения сатурации кислородотерапия проводится под контролем клинических признаков.
Системные кортикостероиды
Прием ОГКС при обострении БА легкой или средней степени тяжести начинается незамедлительно при значительном ухудшении состояния пациента или при условии, что пациент перед поступлением принимал увеличенные дозировки препарата контроля и реливера. Дозировка преднизолона или его эквивалента для взрослых — 1 мг/кг/день (максимально 50 мг) в течение 5–7 дней, для детей — 1–2 мг/кг/день (максимально 40 мг). Прием ОГКС рекомендуется в течение 5–7 дней. Пациентов необходимо предупредить о частых побочных эффектах приема ОГКС (нарушения сна и настроения, повышение аппетита, рефлюкс желудочного содержимого и т. д.).
Препараты контроля астмы
После терапии обострения астмы необходимо увеличение дозировок препаратов контроля (см. выше) на следующие 2–4 недели вплоть до 3 месяцев в зависимости от причины обострения. Пациентам, не получающим терапию контроля, необходимо назначить лечение, включающее ИГКС.
- Рутинное применение антибиотиков при отсутствии убедительных признаков инфекции (лихорадка, гнойная мокрота или рентгенографические признаки пневмонии) при БА не рекомендуется;
- Желательно проводить мониторинг функции дыхания до начала лечения, после применения КДБА и через каждый час до достижения устойчивого уровня (плато) или наилучшего личного показателя пациента вне обострения;
- На основании динамики и полученных значений производится решение о выписке пациента или, напротив, его переводе в ОАиР.
Оказание помощи в ОАиР
Тяжелые обострения бронхиальной астмы, а также сопутствующие жизнеугрожающие состояния являются показанием для нахождения в ОАиР, где пациенту проводится активный мониторинг жизненных функций и имеется больше возможностей для проведения эффективной терапии. Наличие повышенной сонливости, спутанности сознания либо полное отсутствие дыхательных шумов при аускультации легких служат крайне неблагоприятными признаками и требуют повышенного внимания.
Анамнез
Сбор анамнеза ведется по стандартной схеме, представленной выше, однако особое внимание стоит обратить на проводимую ранее терапию и ее эффективность. Выполняется стандартное физикальное исследование: оценка уровня сознания, поведения и речи, частота пульса и дыхания, участие в акте дыхания вспомогательной дыхательной мускулатуры, артериальное давление, наличие/отсутствие сухих хрипов. Учитывая возможности ОАиР, арсенал доступных объективных методов исследования расширяется:
- Исследование функции легких: мониторинг ПСВ или ОФВ за 1 сек проводится при поступлении и каждый час до полного ответа на терапию или до достижения плато;
- Определение сатурации кислорода: пульсоксиметрию желательно проводить всем пациентам, особенно детям ввиду невозможности выполнения у них функциональных тестов. У детей сатурация крови в норме > 95 %, показатели SpO2 < 90 % требуют немедленной агрессивной терапии;
При необходимости (ПСВ или ОФВ1 < 50 % от должного, плохой ответ на начальную терапию, значительное ухудшение состояния) выполняется исследование газов артериальной крови и рентгенография органов грудной клетки (высокая вероятность альтернативного диагноза, выраженные признаки воспалительного процесса, возможность пневмоторакса).
Лечение
Кислородотерапия
Необходимо достигнуть артериальной сатурации кислорода не менее 93–95 % (94–98 % для детей 6–11 лет). Кислород может подаваться через носовые канюли или маску. При тяжелом обострении терапия низкими потоками кислорода с достижением уровня сатурации 93–95 % предпочтительнее подачи высоких потоков 100 % кислорода. После стабилизации пациента проводится его «отучение» от кислорода под контролем сатурации крови.
В очень тяжелых случаях пациентам с обострением БА и признаками тяжелой дыхательной недостаточности (гипоксические расстройства сознания, нарастание одышки и отсутствие дыхательных шумов, нарастающая гиперкапния PaCO2 > 60 мм рт. ст., гипоксемия PaO2 < 60 мм рт. ст и SpO2 < 90 % на фоне подачи кислорода) требуется проведение искусственной вентиляции легких. При ИВЛ применяется техника пермиссивной гиперкапнии, предпочтительнее начинать с режимов с контролем по объему.
Используются низкие дыхательные объемы (6–8 мл/кг), небольшая частота дыхания (около 10 в минуту), высокий пиковый инспираторный поток (до 60 л/мин), удлиненное время выдоха и короткое время вдоха. При риске развития пневмоторакса и трудностях с контролем пикового давления в дыхательных путях переходят к вентиляции в режимах с контролем по давлению. Целью использования данных режимов является контроль пикового давления (не более 40 см вод. ст).
При проведении контролируемой пермиссивной гиперкапнии невысокие уровни PaCO2 хорошо переносятся и не вызывают значительных побочных эффектов (рост внутричерепного давления). Не существует определенного максимально допустимого уровня PaCO2, но желательно не превышать уровни более 100 мм рт. ст.
Ингаляция короткодействующих агонистов бета-2-адренорецепторов
В ОАиР ингаляция может проводиться при помощи небулайзера периодически или непрерывно. Дозировки препаратов КДБА стандартные для начальной терапии (см. выше). Дозировки препаратов для ингаляции через небулайзер: «небула» по 2,5 мл, содержащая 2,5 мг сальбутамола в физиологическом растворе или «небула» 1,5 мг левалбутерола, 1–2 небулы на ингаляцию, повторные ингаляции проводят каждые 20 минут или непрерывно в течение часа.
Адреналин (эпинефрин)
Внутримышечное введение адреналина (эпинефрина) допустимо как дополнение к стандартной терапии при развитии анафилаксии и ангиоэдемы.
Системные и ингаляционные глюкокортикостероиды
Системные глюкокортикостероиды быстро купируют обострение БА и предотвращают ее рецидив. Применение ГКС обязательно при обострении средней степени тяжести у взрослых, детей 6–11 лет и подростков. Терапию начинают с применения ИГКС, а при отсутствии улучшения состояния пациента в течение первого часа от поступления, назначаются системные ГКС, однако данные по эффективности совместного использования ИГКС и ОГКС пока спорные. Особенно важно назначение ОГКС, если начальная терапия КДБА не принесла успеха, обострение развилось на фоне приема ОГКС или ранее для купирования обострения требовалось применение ГКС.
Эффективность оральных форм ГКС сравнима с их внутривенными инъекциями, ввиду этого предпочтительнее использование таблетированных форм (жидкие для детей). Внутривенное введение ГКС может использоваться при наличии у пациента тошноты или рвоты, выраженной одышки, невозможности глотать, а также во время проведения неинвазивной или инвазивной ИВЛ. ГКС применяются в эквивалентных дозах: у взрослых — 50 мг преднизолона однократно утром или 200 мг гидрокортизона, разделенные на несколько доз, у детей — 1–2 мг/кг до максимальной дозировки 40 мг/день. Курс приема для взрослых 5–7 дней, для детей 3–5 дней.
Различные препараты и методики
— Ипратропия бромид: у взрослых с обострением средней или тяжелой степени тяжести при неэффективности проводимой ранее терапии добавление антихолинергического препарата короткого действия (ипратропия бромида) увеличивает скорость восстановления показателей ПСВ и ОФВ1. Проводят его ингаляцию через небулайзер по 0,5 мг каждые 20 минут до трех доз, далее — по необходимости, или с помощью ингалятора (18 мкг/доза) по 8 вдохов каждые 20 минут;
— Аминофиллин и теофиллин: применение данных препаратов при обострении БА не рекомендуется из-за их плохого профиля безопасности и отсутствии доказательств эффективности;
— Препараты магнезии (MgSO4): могут применяться при тяжелом обострении путем однократного внутривенного капельного введения 2 г в течение 20 минут либо как замена в небулайзере изотоническому раствору NaCl 0,9 % (раствор магнезии также должен быть изотоничен).
- У пациентов с БА необходимо избегать применения седативных препаратов ввиду их угнетающего действия на дыхательный центр;
- Преимущества неинвазивной вентиляции легких при обострении на данный момент не доказаны. У тяжелых пациентов, не отвечающих на стандартную терапию, возможно применение гелиево-воздушной смеси;
- В некоторых небольших исследованиях показано улучшение функции легких после приема антагонистов лейкотриеновых рецепторов;
- Применение в стационаре или ОАиР ИГКС/ДДБА спорно и требует дальнейших исследований.
Через час после начала проведения терапии проводится оценка ее эффекта: при ОФВ1 или ПСВ 60–80 % от должного значения возможна выписка пациента, при отсутствии положительной динамики показателей ОФВ1 или ПСВ < 60 % от должного значения или наилучшего личного показателя необходимо продолжить терапию с последующей регулярной оценкой статуса пациента.