Новости
Интервью Натальи Даниловны ГОНЧАРОВОЙ, врача бригады скорой медицинской помощи подстанции №4 г. Луганска Луганского Центра медицины катастроф (ГБУЗ «ЛРЦЭМП и МК» ЛНР) газете «Экспресс-новости» № 17 от 24.04.2024 г.
Скорая помощь это вся моя жизнь, у меня не получается отделить её от личной.47 лет цифра страшная (улыбается), но на самом деле, такое впечатление, что годы слишком быстро пролетели!»

Жители Луганска и ЛНР продолжают делиться впечатлениями о прохождении Курсов первой помощи в Школе медицины катастроф ГБУЗ «ЛРЦЭМП и МК» ЛНР

- Я работаю в магазине мобильной связи и состою в обществе «Динамо», занимаюсь спортом. Многие из моих приятелей, членов клуба, уже прошли такие курсы, поэтому и я решил не отставать. Да, в принципе, любому взрослому человеку нужно посещать курсы первой помощи.

Был случай – на моих глазах в магазине ребенок подавился конфетой, начал задыхаться. У всех вокруг тут же паника, кто-то замешкался, а, что делать – никто толком не знает. Благо, мой коллега, владея навыками оказания первой помощи, тут же ему помог, применив приём Геймлиха, о котором я узнал уже здесь на курсах. Поэтому однозначно – курсы важны, даже необходимы, и пройти их нужно каждому. А вам – спасибо за то, что такие занятия у вас и у нас есть, - рассказал луганчанин Андрей К.
Студенты Института гражданской защиты продолжают курс обучения первой помощи в Луганском Центре медицины катастроф



Инструкторы Школы медицины катастроф проводят теоретические и практические занятия со студентами ФГБОУ высшего образования ЛГУ им. В. Даля «Института гражданской защиты». Каждый день ребята узнают что-то новое, получают важную информацию и необходимые знания. Обучение навыкам оказания первой помощи проходит в рамках учебной программы «Оказание первой помощи пострадавшим в том числе при ЧС». Курс ведут инструкторы школы медицины катастроф.
На днях Роман Цмыкал провел занятие по теме - травмы и кровотечения, а Анна Стрижак ознакомила студентов с правилами первой помощи при ожогах.


Обучение в ГБУЗ «ЛРЦЭМП и МК» ЛНР в целом пройдут более 100 студентов вуза. Экзамены, как теоретические, так и практические, запланированы на конец мая.
Для обучающихся высшего училища физкультуры проведена экскурсия по Луганскому республиканскому Центру медицины катастроф



Заведующая подстанцией №1 г. Луганска Юлия Борисовна Поволоцкая рассказала и показала ребятам, как устроен Луганский республиканский Центр медицины катастроф, его основные задачи и функции. Далее по плану было экскурсия непосредственно по подстанции скорой медицинской помощи, сердцу любой подстанции - центральной оперативной диспетчерской, посещение учебного класса Школы медицины катастроф, где проходят практические занятия, и, конечно же, один самых любимых эпизодов экскурсии абсолютно для всех – знакомство с устройством и работой автомобиля скорой помощи.



Экскурсия проводилась в рамках профориентационной работы и организована совместно с Республиканским Центром занятости населения.

25-26 апреля 2024 г. сотрудники Луганского Центра медицины катастроф примут участие в конференции в г. Сыктывкар
В эти дни там пройдет Всероссийская научно-практическая конференция «Актуальные вопросы медицины катастроф. Опыт регионов», посвященная 10-летию организации Центра медицины катастроф республики Коми. На конференции Луганскую Народную Республику представят врио директора ГБУЗ «ЛРЦЭМП и МК» Евгений Волков и зам. директора Центра по оперативной работе, медицине катастроф и защите населения Виктория Калугина.
В рамках конференции запланированы: секция "Первая помощь в России. Направления развития", совместное заседание профильных комиссий Минздрава России по направлениям «Первая помощь» и «Медицина катастроф».
Организаторами проведения конференции выступили: Федеральный центр медицины катастроф ФГБУ «Национальный медико-хирургический Центр им. Н.И. Пирогова» Минздрава России, Общероссийская общественная организация специалистов в сфере медицины катастроф, Общероссийская общественная организация «Российское общество первой помощи», Общероссийская общественная организация «Российское общество скорой медицинской помощи», ГБУ РК «Территориальный центр медицины катастроф Республики Коми», Медицинский институт ФГБОУ ВО СГУ им. Питирима Сорокина.
Следите за материалами с проведения конференции в наших пабликах.
На базе филиала «Свердловская ССМП» Луганского республиканского Центра медицины катастроф прошел мастер-класс

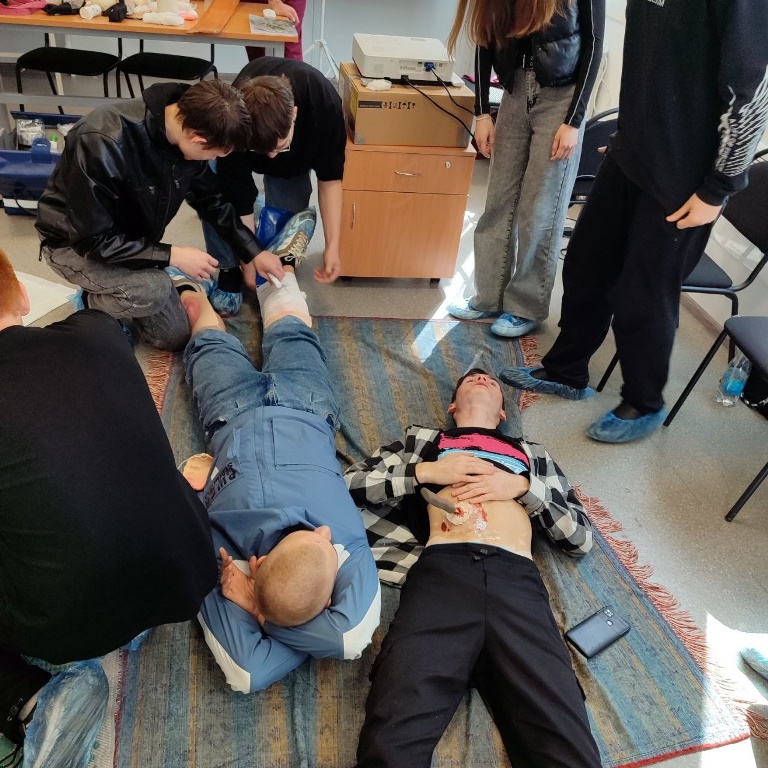

Сотрудники Центра - фельдшеры подстанции №2 г. Ровеньки - провели со студентами Ровеньковского технико-экономического колледжа мастер-класс по оказанию первой помощи. Тема занятия - травмы и кровотечения. Медики - Юлия Науменко, Тарас Зюбанов, Артём Столяренко в теоретической и практической форме познакомили ребят с видами травм и кровотечений, способами остановки кровотечений, правилами наложения повязок, использования жгутов.


15 человек студентов ГБОУ СПО ЛНР «РТЭК», получив информацию, просмотрев обучающий фильм, смогли тут же в процессе смоделированной инструкторами ситуационной задачи с ЧС попробовать закрепить все на практике. По общему мнению участников мастер-класса, именно это способствует наибольшему погружению в материал и работает на результат.













