Алкогольная болезнь печени
Хроническое употребление алкоголя поражает все органы и системы. Но особое внимание стоит уделить алкогольным заболеваниям печени, которые включают в себя различные патологические состояния: от простого стеатоза до воспаления, цирроза и алкогольного гепатита [1].
Алкогольная болезнь печени является одним из наиболее распространенных заболеваний печени в Европе и США [3]. Заболевание может быть вызвано хроническим употреблением алкоголя, превышающим определенное суточное количество. Хроническое употребление > 40 г этилового спирта в день (что составляет 375 мл 13 % вина или > 1 литра 5 % пива) в течение длительного периода времени (годы) ассоциировано с высоким риском развития алкогольной болезни печени [4].
По результатам метаанализа, даже хроническое потребление 12–24 г алкоголя в день ассоциировано с повышенным риском развития цирроза печени (поздняя стадия алкогольной болезни печени), по сравнению с риском для людей, не употребляющих алкоголь [4]. Несомненно, вероятность развития цирроза печени зависит от продолжительности употребления алкоголя [1].
Алкогольная болезнь печени начинается с алкогольной жировой дистрофии, для которой характерен стеатоз печени — накопление триглицеридов в гепатоцитах. У некоторых людей прогрессирует воспаление печени, повреждение гепатоцитов и их увеличение, которое гистологически определяется как алкогольный стеатогепатит (АСГ) [2].
АСГ может развиваться медленно, с постоянным хроническим повреждением печени и воспалением, в конечном итоге приводящим к прогрессирующему фиброзу и циррозу. Впоследствии это может привести к развитию гепатоцеллюлярной карциномы (ГЦК). В дополнение к этому, у людей с АБП (с циррозом или без него) с быстро прогрессирующим АСГ может наблюдаться алкогольный гепатит, который ассоциирован с плохим прогнозом для пациента [2].
.
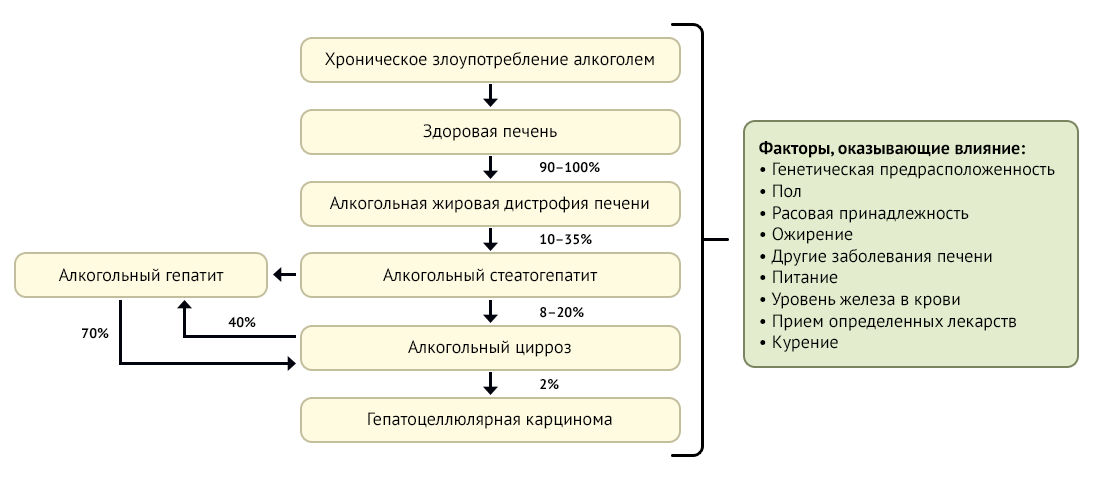
Факторы риска
Существует взаимосвязь между количеством потребляемого алкоголя и риском развития АБП [5]. У большинства (90–100 %) хронических алкоголиков развивается алкогольная жировая дистрофия печени. У 10–20 % хронических алкоголиков развивается прогрессирующая АБП [2].
Среди факторов риска генетическая предрасположенность имеет наибольшее значение [6]. Женщины подвержены большему риску, чем мужчины. АБП у женщин развивается быстрее и при употреблении более низких доз алкоголя [7]. Наличие таких заболеваний печени, как вирусный гепатит B [9] или C [10], наследственный гемохроматоз [11], дефицит α1-антитрипсина [8] и неалкогольный стеатогепатит [12], ассоциировано с повышенным риском развития АБП. Люди с избыточным весом более склонны к токсическому воздействию алкоголя на печень [13]. Прием определенных лекарств или витаминов (парацетамола, изониазида, метотрексата, β-каротина) в сочетании с алкоголем способствует повреждению печени [14]. Курение увеличивает риск развития АБП в три раза [15].
Патофизиологические механизмы
В развитие алкогольной жировой дистрофии печени вносят вклад метаболические изменения, эпигенетические изменения, окислительный стресс и воспаление. Перечисленные факторы воздействуют в первую очередь на гепатоциты и звездчатые клетки печени [2].
Генетика
Среди генов, влияющих на чувствительность организма к хроническому употреблению алкоголя, гены модификаторов нейротрансмиссии (ГАМК) и модификаторов метаболизма алкоголя [17].
Отмечена роль полиморфизмов генов, которые [18]:
• кодируют медиаторы воспаления — фактор некроза опухоли (TNF) и антагонист рецептора IL-1;
• участвуют в ответе на действие эндотоксина — рецептор CD14 и CTLA4;
• участвуют в окислительном стрессе — глутатион-S-трансфераза и марганцевая супероксиддисмутаза.
Ацетальдегид и окислительный стресс
Алкоголь в гепатоцитах окисляется алкогольдегидрогеназой до ацетальдегида, который затем метаболизируется до ацетата. Цитохром P450 2E1 (CYP2E1) — фермент, присутствующий в эндоплазматической сети и митохондриях гепатоцитов, метаболизирует алкоголь до ацетальдегида в присутствии кислорода и НАДФ. Такой метаболизм алкоголя является альтернативным, и этот путь запускается при хроническом злоупотреблении алкоголем (рис. 3) [2].
.
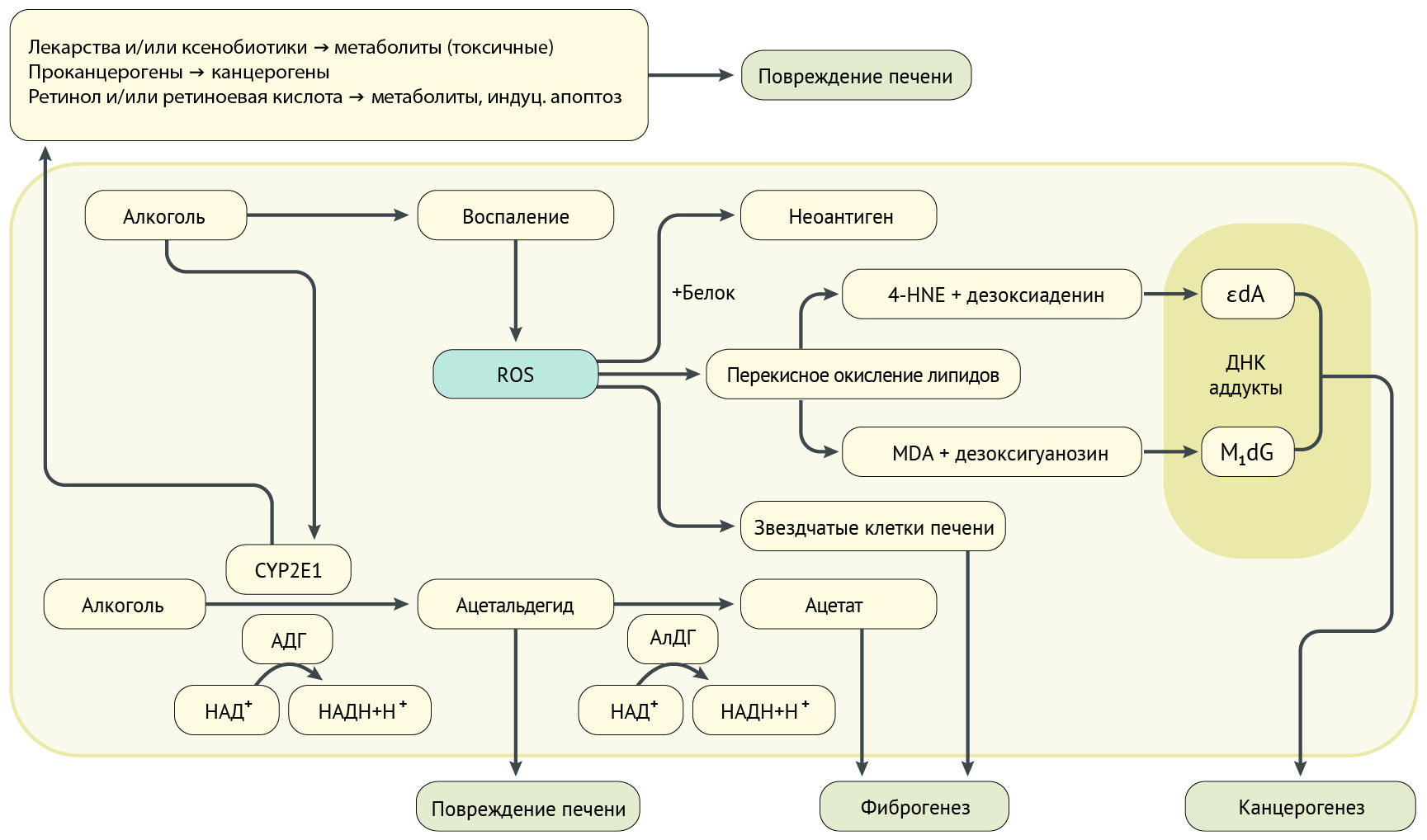
Ацетальдегид является токсичным и канцерогенным, связывается с белками, что приводит к структурным и функциональным изменениям митохондрий и микротрубочек и индуцирует образование неоантигенов [19]. Структурные изменения митохондрий приводят к снижению образования АТФ в дыхательной цепи, выработке активных форм кислорода (АФК) и окислительному стрессу, а также снижению активности ацетальдегиддегидрогеназы [16].
Эпигенетика
Эпигенетические изменения включают ацетилирование и фосфорилирование, а также гипометилирование ДНК и изменения микроРНК [2].
Алкоголь модулирует ацетилирование гистона H3 посредством индукции активности гистонацетилтрансферазы и ингибирования гистондеацетилазы [20]. Происходит снижение экспрессии Sirtuin 1 в гепатоцитах, что приводит к усиленной регуляции стерол-регуляторного элемента, связывающего фактор транскрипции 1 (SREBP1), и последующему снижению метаболизма липидов в печени, что ведет к ожирению печени [21]. Связанная с алкоголем эпигенетическая регуляция также изменяет функции иммунных клеток. У макрофагов повышается активность гистондеацетилазы 11, регулятора IL-10, и это способствует снижению продукции противовоспалительного цитокина IL-10 [22].
Стеатоз печени
Первым патофизиологическим ответом на хроническое употребление алкоголя является накопление жира (в основном триглицеридов, фосфолипидов и сложных эфиров холестерина) в гепатоцитах (стеатоз печени), что может привести к алкогольной жировой дистрофии печени. Потребление алкоголя может вызывать накопление жира в печени при помощи нескольких механизмов [2]:
1. Потребление алкоголя повышает отношение восстановленного НАД к окисленному НАД (НАДН/НАД+) в гепатоцитах, что препятствует β-окислению жирных кислот в митохондриях и приводит к стеатозу.
2. Потребление алкоголя может усиливать экспрессию в клетках печени SREBP-1c — транскрипционного фактора, который стимулирует экспрессию липогенных генов, что приводит к увеличению синтеза жирных кислот.
3. Алкоголь инактивирует рецептор-α, активируемый пролифератором пероксисом (PPARα). Это ядерный гормональный рецептор, который усиливает экспрессию многих генов, участвующих в транспорте и окислении свободных жирных кислот.
4. Употребление алкоголя вызывает липолиз и гибель адипоцитов, что приводит к повышению концентрации циркулирующих жирных кислот и их последующему накоплению в печени.
Ингибирование убиквитин-протеасомного пути
Убиквитин-протеасомный путь регулирует переваривание белка в клетке. С помощью данного механизма регулируются многие функции клеток печени, включая контрольные точки клеточного цикла и активацию факторов транскрипции (например, NF-κB и индуцируемый гипоксией фактор 1α — HIF1α). Потеря протеасом или ингибирование этого пути может привести к повреждению клеток, апоптозу и накоплению агрегированных цитокератинов в печени. Экспрессия генов в клетках печени зависит от активации транскрипционного фактора протеасомами. Активация определенных генов может ингибировать воспалительную реакцию печени и реакцию на гипоксическое повреждение [2].
Фиброз и цирроз
Фиброгенез является предпосылкой развития цирроза печени. На более поздних стадиях АБП характеризуется развитием запущенного фиброза, что ассоциировано с ранней смертностью пациентов. Фиброз при AБП отличается накоплением перицеллюлярного и перисинусоидального матрикса. Постоянное употребление алкоголя усугубляет процесс [2].
Алкоголь, ацетальдегид и АФК (рис. 2) могут способствовать фиброгенезу печени, стимулируя иммунные клетки к образованию профиброгенных медиаторов. Алкоголь-опосредованное ингибирование нескольких антифиброзных путей также способствует фиброзу печени. Когда фиброз прогрессирует, печень становится цирротической и состоит преимущественно из соединительной ткани, что приводит к серьезному нарушению печеночного кровотока из-за сужения сосудов в печеночной дольке. В результате могут развиться осложнения: портальная гипертензия, асцит, варикозное расширение вен пищевода, печеночная недостаточность [2].




