Новости
В пилотном исследовании группа ученых из Техаса обнаружила кристаллические частицы диоксида титана – наиболее распространенного белого пигмента в продуктах ежедневного использования – в поджелудочной железе диабетиков. Это может свидетельствовать о том, что вещество связано с болезнью.
Диоксид титана (TiO2) в норме не содержится в тканях человека, в отличие от множества других соединений металлов. Группа ученых исследовала девять препаратов поджелудочной железы, донорами которых были диабетики, и три от здоровых людей. У последних в органе не было определяемых частиц TiO2, тогда как он был найден в препаратах, полученных от диабетиков. Об этом ученые сообщают на страницах журнала Chemical Research in Toxicology.
«Наши находки поднимают вопрос о вероятности того, что сахарный диабет 2 типа может быть хронической воспалительной болезнью поджелудочной железы, связанной с кристаллами, наподобие таких болезней легких, как асбестоз и силикоз», - говорит автор исследования Адам Геллер (Adam Heller), профессор кафедры химической инженерии Техасского университета в Остине.
В середине XX века диоксид титана заменил токсические пигменты на основе свинца. Он стал наиболее широко используемым белым пигментов в красках и пище, медикаментах, зубной пасте, косметике, пластике и бумаге.
Согласно ВОЗ, в течение последних сорока лет количество людей с сахарным диабетом 2 типа выросло в четыре раза. Хотя основными факторами риска заболевания считаются ожирение и возраст, исследование Геллера показывает, что увеличение использования диоксида титана также может быть связано с быстрым увеличением количества заболевших.
«Возросшее использование диоксида титана в течение последних пяти десятилетий могло быть фактором эпидемии сахарного диабета 2 типа. Частицы, связанные с диабетом, которые мы находим в поджелудочной железе, состоят из кристаллов TiO2, которые используются в подкрашивании пищи и лекарств, в красках. Они могут попадать в поджелудочную железу с кровотоком. Исследование поднимает вопрос о возможности связи роста заболеваемости с глобальным увеличением использования пигмента TiO2», - говорит Геллер.
Учитывая возможность огромного влияния этих данных, Геллер хочет повторить это исследование на большей выборке участников. Эта работа уже начата.
Врачи в ужасе от количества людей, которые с помощью Интернета занимаются самолечением. Но иногда Всемирная сеть может оказать помощь тем, кто пытается поставить себе диагноз по симптомам.
В четырёх российских регионах – Санкт-Петербурге, Ленинградской области, Москве и Татарстане – стартует второй этап проекта по ранней диагностике болезни Бехтерева, или анкилозирующего спондилоартрита. Основная цель программы – выявление новых случаев на самых первых стадиях, когда потенциальные больные только ищут симптомы своего состояния в Интернете. Главная особенность проекта – в сотрудничестве с тремя ведущими медучреждениями страны его запускают пациенты: те, кто не понаслышке знает об этом заболевании.
Неверный диагноз. Итог – инвалидность
Наблюдения врачей из НИИ ревматологии имени В. А. Насоновой говорят о том, что при болезни Бехтерева даже на приём к терапевту люди приходят только через 15 месяцев после дебюта – появления первых симптомов. В случае со спондилоартритом – это боли в спине и суставах, ограничение подвижности. Обычно такие признаки связывают с остеохондрозом или неврологическими нарушениями, поэтому часто терапевт даёт направление не к ревматологу, а к неврологу или ортопеду. В результате у нужного специалиста пациент оказывается лишь спустя 70 месяцев после начала заболевания, что ведёт к потере драгоценного времени, когда недуг проще остановить и избежать серьёзных осложнений.
«Моя история развивалась именно по такому сценарию, – говорит президент Межрегиональной общественной благотворительной организации инвалидов «Общество взаимопомощи при болезни Бехтерева» Алексей Ситало. – Спондилоартрит проявил себя, когда мне было 13, но верный диагноз был поставлен лишь в 20 лет. Без должного лечения болезнь прогрессировала очень быстро, и из-за этого уже в 22 года мне пришлось заменить тазобедренный сустав».
Интернет выведет на нужного специалиста
Печальный пациентский опыт стал для Общества взаимопомощи при болезни Бехтерева поводом к тому, чтобы реализовать проект по раннему выявлению спондилоартрита. Как известно, сейчас многие первым делом идут не в поликлинику, а в Интернет, пытаясь самостоятельно поставить себе диагноз. Именно на таких пациентов и рассчитана разработанная программа.
Совместно с экспертами по спондилоартриту организаторы проекта проанализировали наиболее частые поисковые запросы тех, кто обеспокоен характерными болями в спине и суставах. В общей сложности было выделено 1500 слов и словосочетаний.
«Мы запускали пробные кампании в прошлом году, – продолжает Алексей Ситало. – Результаты не очень утешительные для нашей системы здравоохранения. Оказалось, что из 1000 прошедших тест более 600 нуждаются в консультации ревматолога».
Как говорит глобальная статистика, в мире около 1% населения страдает от болезни Бехтерева. По данным Мин¬здрава РФ, в стране 33 тысячи человек, по клиническим данным – около 140 тысяч. Если же провести подсчёты согласно мировой статистике, пациентов должно быть около 1,5 млн. Скорее всего, некоторые из них сейчас безуспешно лечатся от других заболеваний. И поставить им правильный диагноз – одна из важнейших задач. Первый этап проекта предоставил статистические данные, в каком направлении можно вести дальнейшую работу. Так, опрос показал, что помимо поражений позвоночника, тазобедренного сустава и других скелетных проявлений многие также сталкиваются с воспалительными заболеваниями кишечника, псориазом и болезнями глаз.
Не упустить окно возможностей
«Мы запускаем второй этап нашего большого проекта. Здесь мы задействуем не контекстную рекламу, а медицинских специалистов: офтальмологи будут направлять на наш сайт пациентов, у которых есть предрасположенность к болезни Бехтерева или симптомы воспалительных болей в спине. К проекту подключены эксперты Высшей школы экономики. Мы хотим подсчитать, насколько экономически эффективна подобная работа для предотвращения инвалидизации в масштабе четырёх регионов. Мой пример красноречиво показывает, что такое высокая активность болезни и как важно не упустить терапевтическое окно возможностей – короткое время, когда благодаря системному подходу к лечению заболевания можно избежать тяжёлых последствий. Лечебная физкультура и своевременное лечение, в том числе с использованием высокотехнологичных препаратов, помогают пациентам сохранять здоровье, а государству – уйти от лишних трат», – подытоживает президент Общества взаимопомощи при болезни Бехтерева.
В 1886 году, на следующий год после открытия Вильгельмом Рентгеном «икс-лучей», знаменитый изобретатель Томас Эдисон публично заявил, что намерен получить первый рентгеновский снимок «живого мозга». Однако уже через несколько недель работы великому ученому пришлось признать свою неудачу — ему так и не удалось создать технологию, позволяющую рентгеновским лучам «заглянуть внутрь» плотной структуры костей черепа, сохранив данные о мягкой ткани мозга. Такой возможности человечеству пришлось подождать до конца следующего века, пока в 1972 году не был предложен метод компьютерной томографии.
Сегодня компьютерная томография считается сравнительно простым, доступным и повсеместно используемым диагностическим методом.
Принцип получения изображений
Компьютерная томография базируется на рентгеновском излучении и его детектировании. Это особый вид электромагнитного излучения, которое способно проходить через непрозрачные для обычного света среды. Нужно помнить, что это излучение:
- ослабляется в среде (тканях) тем больше, чем плотнее среда, сквозь которую они прошли;
- имеет непрямой ионизирующий эффект, то есть отрыв электронов от атомов вещества, через которое проходит рентген-излучение, что и обуславливает лучевую нагрузку на пациента при исследовании;
Итак, у нас есть излучатель (рентген-трубка) и детекторы. Наша задача — получить визуальное отображение аксиальных «срезов» тела пациента. Как нам нужно направить луч?
Линию, по которой проходит рентген-излучение от излучателя к детектору, как правило называют осью х, линию, которая проходит, проще говоря, от «право» к «лево» для пациента — осью у, а линию «верх-низ» пациента, то есть толщину среза — осью z.
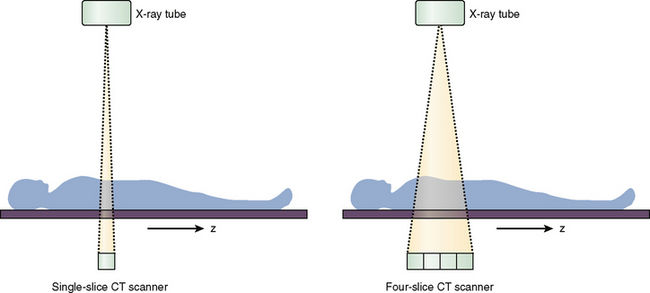
Рисунок 1 | Направление рентгеновского луча в компьютерном томографе.
В современном компьютерном томографе рентгеновская трубка совершает спиральное вращение вокруг тела пациента в аксиальной плоскости, постоянно генерируя излучение. Если точнее, трубка вращается по кругу, и одновременно с этим непрерывно смещается вперед или назад стол с пациентом.
В традиционных пошаговых томографах происходит цикл «вращение — шаг стола — вращение».
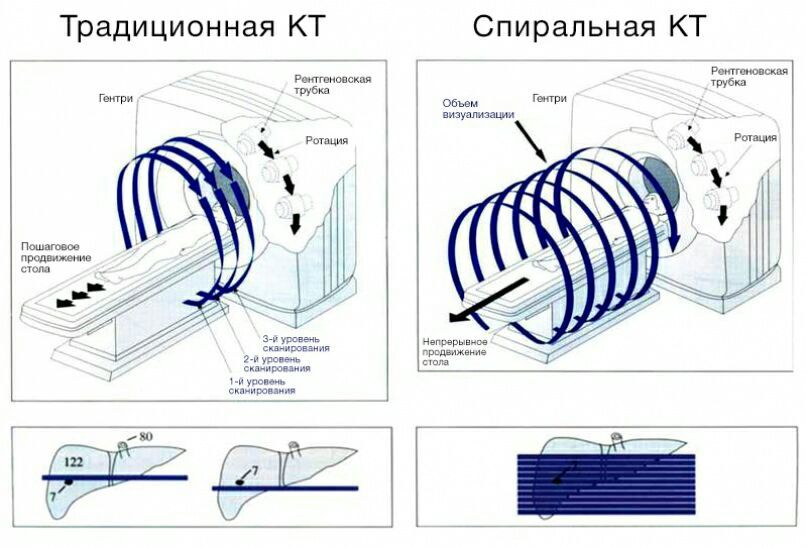
Рисунок 2 | Принцип работы спирального и пошагового томографов. Основным недостатком пошаговых томографов является то, что при небольшом размере образования и разной глубине вдоха пациента образование может быть «пропущено».
При этом пучок излучения сформирован в виде тонкого веера — широкий по оси у, узкий по оси z. Проходя сквозь тело пациента, рентгеновское излучение ослабляется соответственно плотности ткани, через которую оно прошло, затем попадает на детекторы и регистрируется.
Детекторы в современных КТ-аппаратах расположены в несколько рядов, причем наружный ряд шире, чем внутренний. Это позволяет многократно регистрировать излучение от каждого среза, получая более точные данные и сокращая время исследования. В наиболее распространенных на сегодня типах томографов может быть от 4 или 16 до 320 рядов детекторов, как в представленном фирмой Toshiba в 2007 году AQUILION ONE. Когда Вы слышите термин «16-срезовый КТ», имеется ввиду именно количество рядов детекторов. Детекторы могут быть расположены дугой напротив излучателя и вращаться одновременно с трубкой (томографы 3-го поколения), а могут быть неподвижными и занимать всю окружность, в то время как вращается только рентгеновская трубка (4-е поколение томографов).
А дальше начинается именно то, за что Аллан Кормак и Годфри Хаунсфилд получили Нобелевскую премию в 1979 году: на основе имеющихся данных о том:
- какое количество излучения покинуло рентгеновскую трубку;
- какое количество излучения зарегистрировалось детекторами;
- и где находилась трубка и детекторы в каждый момент времени происходит реконструкция и построение изображений с помощью итеративных алгоритмов.
Для реконструкции используются данные от каждого луча, который проходил через выбранное поле обзора от трубки до детектора. Коэффициент ослабления для каждой точки изображения рассчитывают с помощью усреднения значений ослабления для всех лучей, пересекающих эту точку. Полученные таким образом данные называют исходными, или «сырыми». Эти необработанные данные уже представляют изображения срезов, отображенные в оттенках серой шкалы, однако нуждаются в дальнейшей обработке.
Шкала Хаунсфилда
Во время реконструкции изображения каждому пикселю приписывается числовое значение, выраженное в единицах ослабления, или единицах Хаунсфилда, которое определяется тем, насколько ослабляется луч, проходя через данный воксель (единицу объема) — проще говоря, эта шкала показывает примерную плотность вещества.
Само изображение среза, каким мы увидим его на экране, получается благодаря тому, что каждый пиксель будет отображен каким-то оттенком серого в зависимости от плотности вокселя и настроек окна. Шкала Хаунсфилда начинается со значения –1000 HU (hounsfield unit) для воздуха, значение 0 HU задано для воды, жир занимает значения от –120 до –90 HU, нормальная ткань печени — 60–70 HU, кровь — 50–60, костная ткань — 250 и выше. Верхний предел шкалы колеблется от +1000 до более чем +3000 для разных томографов. Программы-просмотрщики КТ-изображений всегда имеют возможность вычислить среднюю плотность выделенной области, ведь отличить разницу в 10–15 HU «на глаз» трудно, но разница эта может быть значима, например, для диагностики жирового гепатоза, степени накопления новообразованием контраста и т. д.
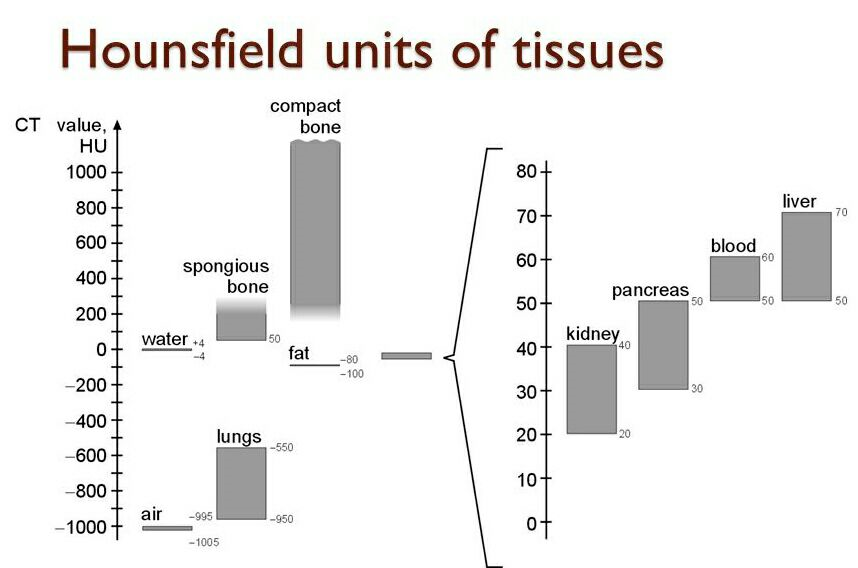
Рисунок 3 | Шкала Хаунсфилд.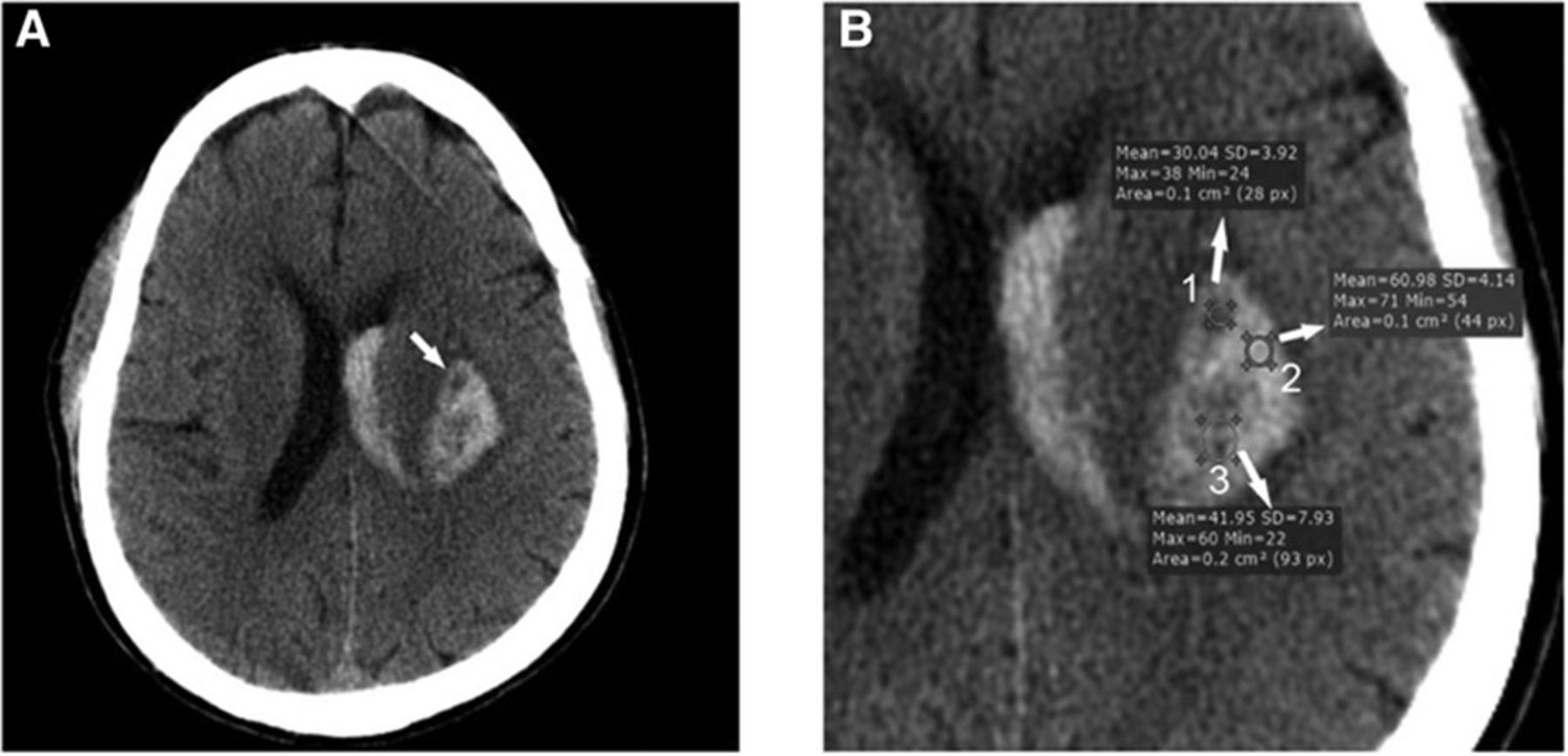
Рисунок 4 | Измерение плотности внутримозговой гематомы: область под номером 2 имеет типичную для крови плотность 60 HU. Область сниженной плотности под номером 1 представляет собой проявление симптома «черной дыры», область под номером 3 представлена как пример неправильного проведения денситометрии (выделенная область интереса гетерогенна, поэтому полученные показатели усреднены).
Функция «окон»
Для визуальной оценки КТ-изображений важны настройки окна. Дело в том, что человеческий глаз не способен различить несколько тысяч оттенков серого, и, чтобы различить близкие по значению плотности, но все же разные структуры, изображение рассматривают в определенном окне. Например, ширина костного окна — 2000 HU, уровень — 500 HU. Это значит, что структуры плотностью 500 HU отобразятся на экране в виде средне-серого цвета, значениям 500 HU до –500 HU будут присвоены оттенки от средне- до очень темно-серого, а структуры плотностью ниже –500 будут отображены слишком темными, чтобы четко их дифференцировать. Структуры плотность выше 1500 HU будут, соответственно, слишком светлыми.
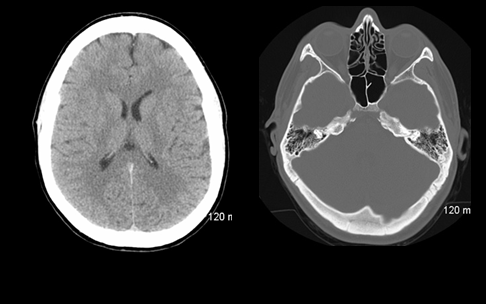
Рисунок 5 | КТ-сканы мозга в «мозговом» (слева) и «костном» (справа) окнах.
Обработка данных
Но вернемся к полученным в результате первичной алгебраической обработки данным. Если перевести «сырые» данные в изображения, то они получатся нерезкими и с размытыми контурами, поэтому для дальнейшей обработки применяют математическую фильтрацию с усилением контуров (конволюцию).
Кернель, или ядро конволюции заложено в протоколе исследования и обработки данных, однако радиолог может менять его по своему усмотрению, задав более «жесткий» или «мягкий» кернель. Например, для сред с высоким естественным контрастом (ткань легкого, костные структуры) применяют жесткий кернель, для органов брюшной полости (низкий естественный контраст) — мягкий. Есть возможность применить разный кернель конволюции к одному и тому же массиву сырых данных, например, после сканирования головы пациента с подозрением на черепно-мозговую травму создать одну серию изображений с жестким кернелем для четкой визуализации костей черепа, а вторую — с мягким кернелем, на ней будут хорошо визуализированы ткани мозга и мозговых оболочек. Каждая серия анализируется радиологом отдельно.
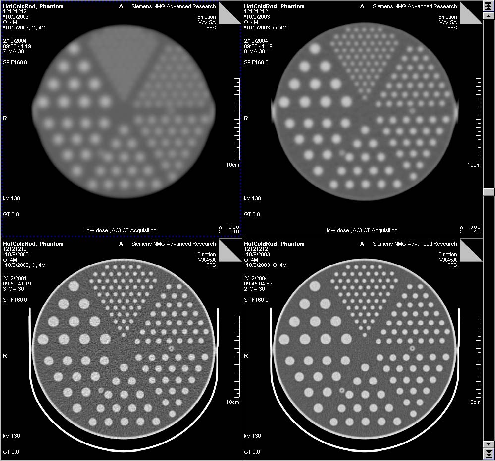
Рисунок 6 | КТ-сканы «фантома» (объекта с внутренней структурой разных плотностей, который используется для проверки и калибровки томографа) с разным кернелем конволюции и силой тока: слева вверху — «мягкий» кернель AC05s, справа вверху — AC10s, внизу слева — стандартный кернель B40s с низкой силой тока 30 mAs, внизу справа — стандартные кернель и сила тока 140 mAs.
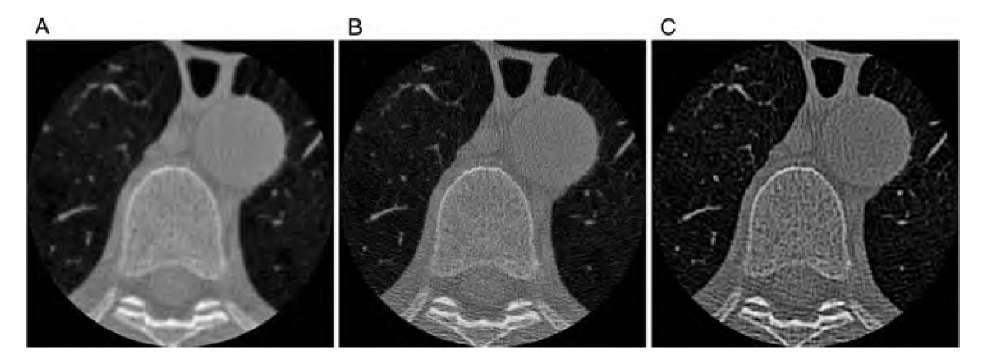
Рисунок 7 | КТ-сканы грудного отдела позвоночника с применением «стандартного» (А), «костного» (В) и «легочного» (С) кернеля конволюции.
Еще один важный параметр реконструкции изображения — толщина среза. Его минимальное значение определено параметрами сканирования (проще говоря, толщиной луча). Тонкие срезы используются там, где нужно визуализировать множество мелких контрастных структур — например, при томографии височной кости. Однако чем тоньше срезы, тем больше время сканирования и лучевая нагрузка на пациента.
Для дальнейшей удобной работы с полученными после первичной обработки исходными данными в КТ применяют инструменты постпроцессинга. Наиболее частые — это мультипланарная реконструкция (MPR), позволяющая из аксиальных сканов построить коронарные и саггитальные изображения.
Проекция максимальной интенсивности (MIP) строится таким образом: для каждой координаты XY представлен только пиксель с наивысшим номером Хаунсфилда вдоль оси z, так что в одном двумерном изображении наблюдаются все самые плотные структуры в данном объеме. MIP используют для визуализации костных структур или контрастированных сосудов.
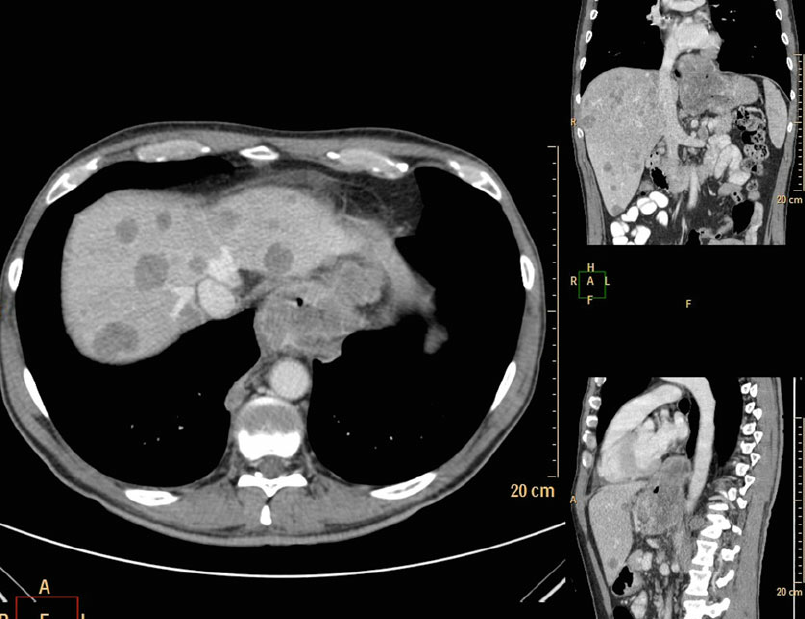
Рисунок 8 | Аксиальный КТ-скан (слева), корональная (вверху) и саггитальная (внизу) мультипланарные реконструкции.
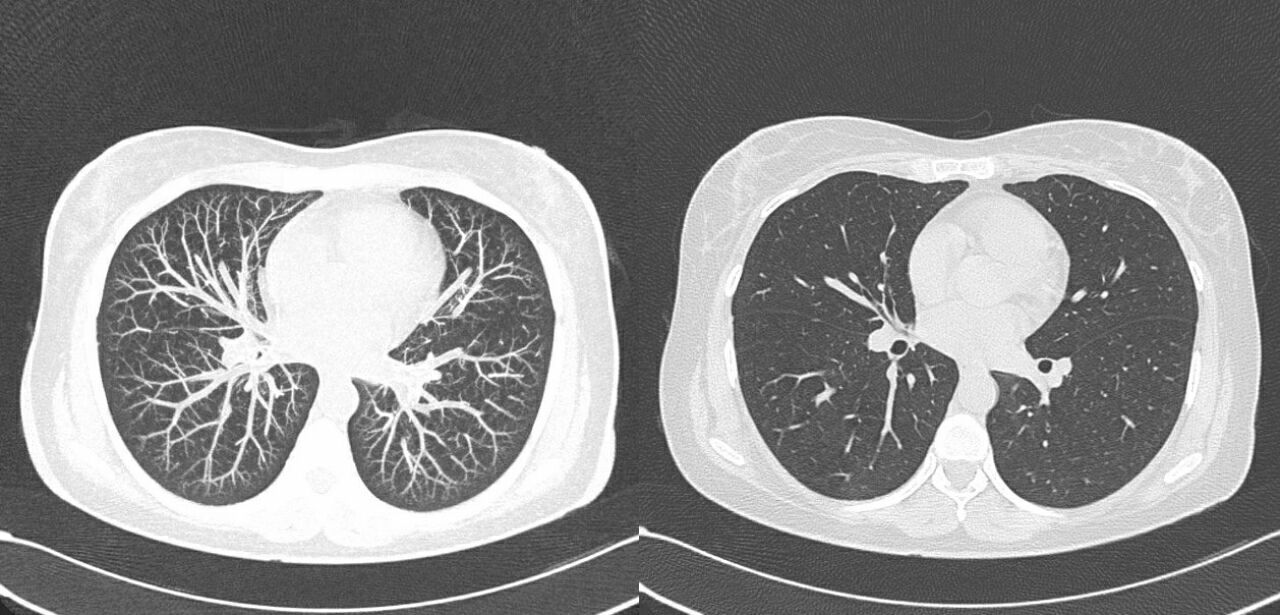
Рисунок 9 | Использование MIP для просмотра ангиографии сосудов легких.
Другой метод — 3D-рендеринг, позволяющий восстановить из исходных данных, подходящих по определенный критерий (чаще всего это также структуры наивысшей плотности — кости и кровь, содержащая контрастное вещество) трехмерную модель. Работая на станции, радиолог может рассматривать модель со всех сторон и «отрезать» лишние фрагменты изображений. Одним из видов 3D рендеринга является виртуальная эндоскопия — технология, позволяющая вывести в трехмерном изображении полый орган (чаще всего проводят виртуальные колоноскопию и бронхоскопию). Это исследование не заменяет реальной скопической процедуры, но может предоставить дополнительные данные или помочь в планировании реальной процедуры.
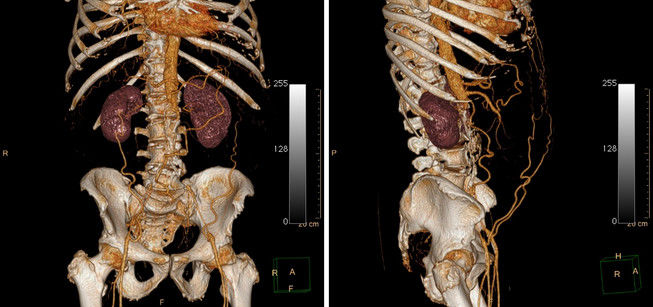
Рисунок 10 | 3D-реконструкция КТ органов брюшной полости и малого таза.
4D-рендеринг широко используется в основном для КТ-исследования сердца. Для этой технологии необходим томограф с возможностью синхронизировать сканирование и сердечный ритм пациента; используются томографы 4-го поколения либо мультисрезовые томографы с количеством детекторов от 64 и выше. Сканирование проводится в разные фазы сердечного цикла, затем из полученных изображений строится последовательность 3D-моделей, по очереди соединенных в «фильм», позволяющий отследить изменения во время сердечного цикла.
Использование контрастных веществ
Для большинства исследований в КТ используют контрастные вещества (КВ) — вещества, содержащие йод и повышающие значения плотности среды, в которой находятся. В настоящее время выделяют ионные и неионные, мономерные и димерные йодсодержащие рентгеноконтрастные средства. Ионные КВ имеют повышенную осмолярность и в настоящее время не рекомендованы для парентерального контрастирования из-за высокой частоты побочных эффектов. Ионные КС могут быть использованы для перорального контрастирования, сиалографии (контрастирования слюнных желез) и т.д.
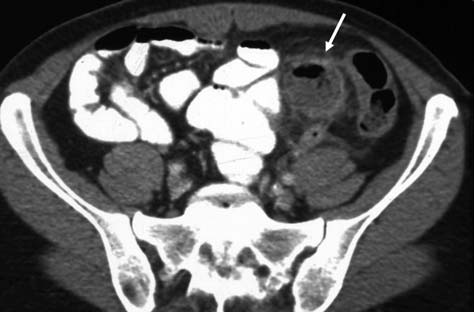
Рисунок 11 | КТ-сканы органов брюшной полости с пероральным контрастированием кишечника (стрелкой показан дивертикул стенки кишечника).
Существуют различные методики КТ-исследования с помощью контрастного препарата.
«Классическая» многофазная КТ предполагает введение сравнительно большого (обычно от 70 до 120 мл) контрастного средства со скоростью 3–4 мл/с. За этим следует несколько сканирований нужной области в определенные моменты времени — фазы. Например, исследование печени при подозрении на новообразование чаще выполняется в нативную (бесконтрастную), артериальную (контрастное вещество преимущественно в артериях, 15–40 с от начала введения), портовенозную (КВ в системе портальной вены и печеночных венах, 55–60 с) и отсроченную, или паренхиматозную (несколько минут после введения КВ) фазы. Полученные изображения позволяют не только оценить анатомию сосудов органа, но и дифференцировать найденные образования по характеру накопления КВ.
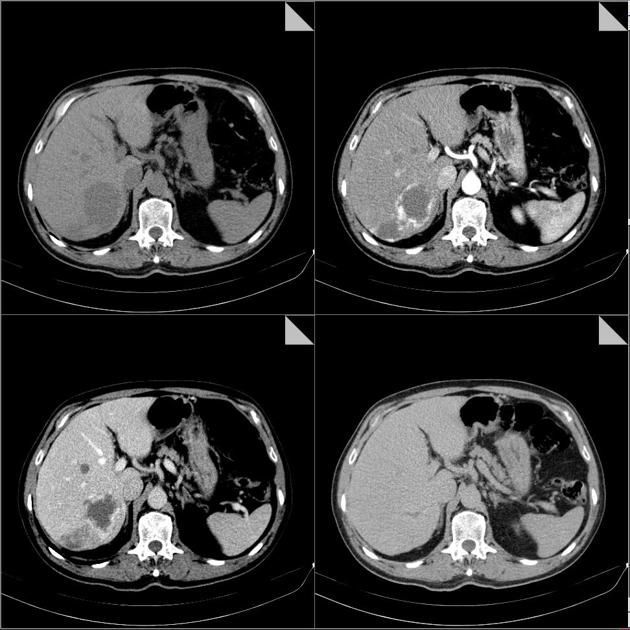
Рисунок 12 | Трехфазная контрастная КТ пациента с гигантской гемангиомой печени: нативная (бесконтрастная) фаза вверху слева; вверху справа — артериальная фаза; внизу слева — портовенозная фаза; внизу справа — отсроченная (5 мин).
Образование активно накапливает контраст и в артериальную фазу «светится» интенсивнее остальной паренхимы, а в венозную и отсроченную фазы контраст «вымывается» и образование выглядит менее плотным или таким же по плотности, как и остальная паренхима? Вероятно, это гиперваскулярная опухоль или метастаз. Не накапливает контраст (или накапливает в пределах 10 HU) и выглядит гиподенсным во всех фазах? Скорее всего, это киста.
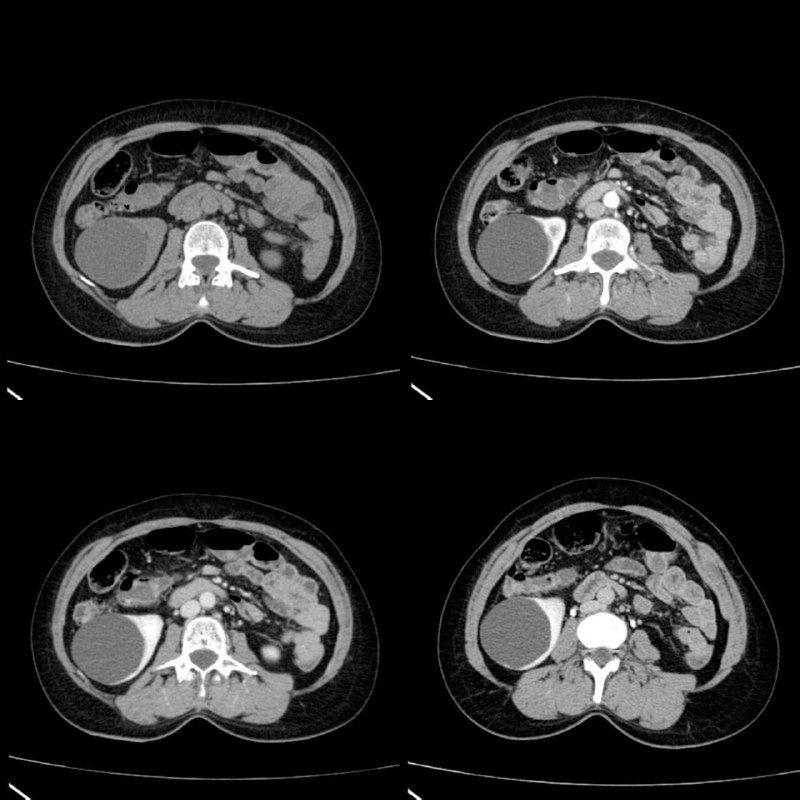
Рисунок 13 | Трехфазная контрастная КТ пациента с простой кистой почки: нативная фаза — вверху слева; вверху справа — кортикальная почечная фаза; внизу слева — паренхиматозная фаза; внизу справа — экскреторная.
Учитывая накопление КВ в определенных фазах, характер этого накопления, а также размеры, расположение и структуру образования, рентгенолог делает предположение о характере образования. Внутривенное контрастирование используется также для проведения КТ-ангиографии.
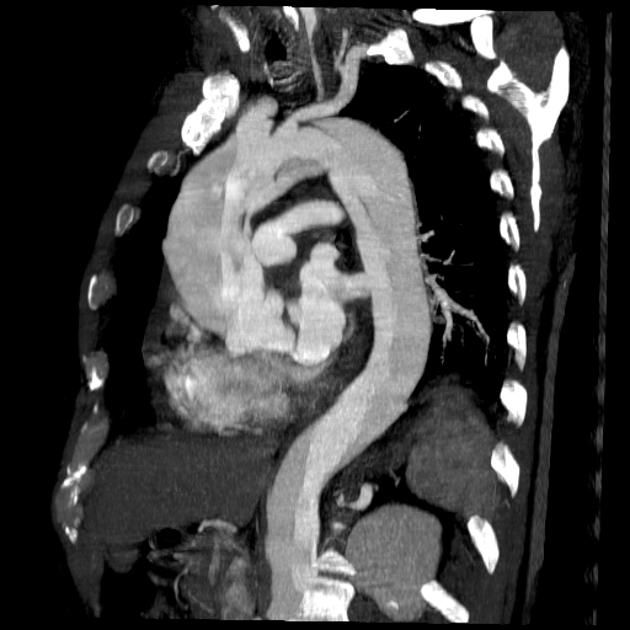
Рисунок 14 | КТ-аортография у пациента с диссекцией аорты.
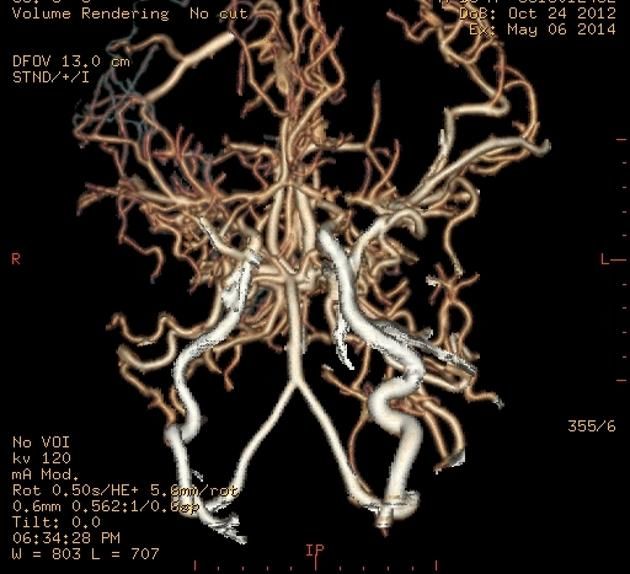
Рисунок 15 | КТ-ангиография артерий головного мозга у пациента с болезнью МояМоя (3D-реконструкция).
Перфузионная КТ используется чаще всего для диагностики нарушений мозгового кровообращения и нарушений перфузии миокарда, а также для оценки раннего ответа на химиотерапию. Эта методика позволяет отграничить зону некроза от пенумбры — зоны обратимой ишемии. Перфузионная КТ может быть выполнена на любом мультиспиральном компьютерном томографе, однако, чем больше он имеет детекторов, тем большую зону можно охватить при сканировании. Начальным этапом выполнения перфузионной КТ является нативное сканирование для исключения геморрагии, а также для выявления иной патологии головного мозга. Перфузионная КТ выполняется после внутривенного болюсного введения 40–50 мл контрастного препарата и 2030 мл физиологического раствора со скоростью 5 мл/с. После внутривенного болюсного введения контрастного препарата выполняются многократные сканирования на одном или нескольких уровнях, следующие друг за другом с минимальными промежутками времени или при непрерывной работе рентгеновской трубки. Общая длительность перфузионного исследования составляет около 1 минуты. Для получения графика контрастного усиления (зависимость плотности в единицах Хаунсфилда от времени) для каждого воксела в зоне интереса необходимо зарегистрировать множественные фазы и находить зоны, где скорость кровотока и времени транзита контрастного препарата не соответствуют объему кровотока, что и будет показателем обратимой ишемии.
Правила чтения томограмм
Можно выделить несколько основных факторов, затрудняющих чтение томограммы:
- бывает сложно «узнать» анатомические структуры, рассматривая их на аксиальных срезах;
- затруднять чтение могут также артефакты (чаще встречаются артефакты от движения и от присутствия металлических объектов);
- эффекты частного объема.
О последних поговорим подробнее.
Один срез на экране представляет собой плоскостное изображение, построенное из пикселей. Однако нужно помнить, что одному пикселю на экране соответствует трехмерный воксель в реальной жизни и толщина этого вокселя соответствует толщине среза.
Допустим, в срез попала структура, которая на всей толщине среза имеет приблизительно одинаковую ширину, например, сосуд. В данном случае проблем не возникает, и структура будет иметь на сканах четкие контуры.
Но что, если срез пришелся на край позвонка? В воксель попала часть позвонка и часть межпозвоночного диска. Они имеют разную плотность и немного разные размеры. Полученные от вокселей данные суммировались, и в результате на скане появляется структура с нечеткими контурами, плотность которой представляется средней между плотностью позвонка и диска.
Еще один пример: округлой формы образование или лимфоузел. При сканировании в срез попадает часть лимфоузла, остальное — окружающая жировая клетчатка. На скане мы увидим нечеткую округлую структуру, а если захотим измерить ее плотность, значения будут средними между реальной плотностью узла и плотностью жира.
Если структура имеет коническую форму и сужается «в срезе», она также будет иметь нечеткие контуры. Примером может служить размытость контуров почки в области полюсов на томограммах. Такая же размытость появится, если, например, сосуд «делает поворот» в срезе.
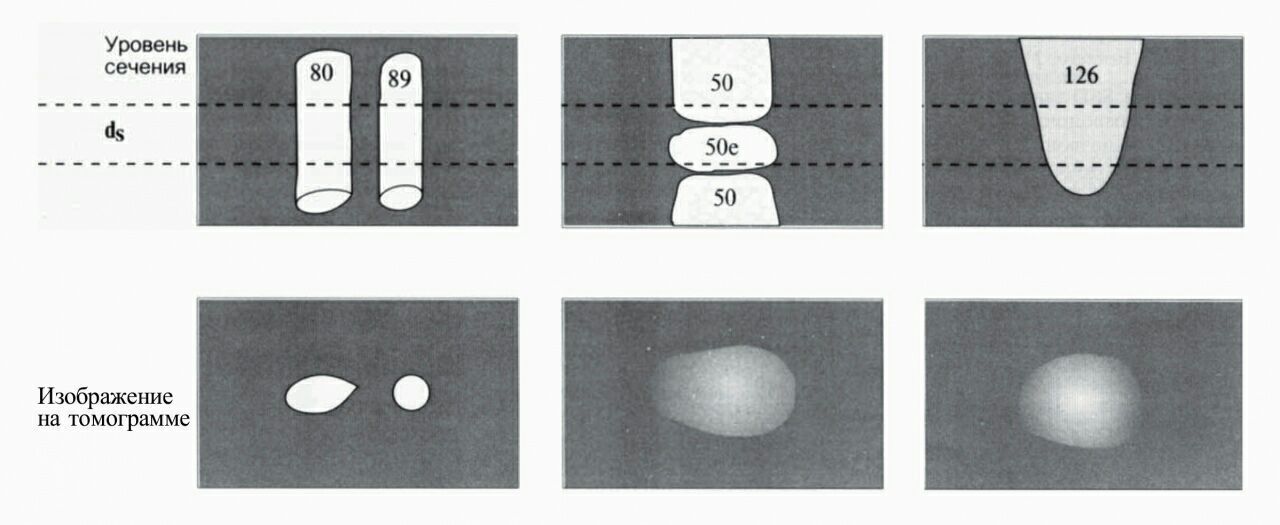
Рисунок 16 | Эффеты частного объема.
Исходя из сказанного, можно дать несколько советов врачу или студенту, который осмелился открыть диск с КТ-исследованием пациента (или сесть за рабочую станцию радиолога) и проанализировать его самостоятельно:
- Пользуйтесь атласами посрезовой и специальными атласами КТ- и МРТ-анатомии наряду с обычными анатомическими атласами;
- Не анализируйте только аксиальные срезы: откройте в просмотрщике несколько окон и прослеживайте интересующую Вас структуру на аксиальных, сагиттальных и корональных срезах одновременно;
- Внимательно проанализируйте изображения, используя разные настройки окна, чтобы хорошо изучить структуры разной плотности; вы увидели образование легкого в «легочном» окне? Изучив его, перейдите в «костное» окно, чтобы выявить возможные метастазы в костные структуры;
- Также внимательно изучите исследование в разных фазах контрастирования; некоторые образования могут иметь схожую с окружающей тканью плотность на бесконтрастных сканах и выделяться только после введения контраста;
- Узнайте, проводилось ли пациенту контрастное исследование до проведенного КТ? Возможно, он проходил рентгеноскопию с применением сульфата бария, и увиденные вами ярко светящиеся области в просвете кишечника — это остатки бариевой взвеси; пациенту проводилось КТ с внутривенным контрастированием накануне? Контрастное вещество может оставаться в мочевыводящих путях (время его выведения зависит от используемого препарата и функции почек), а в случае экстравазации контрастного средства — в мягких тканях пациента;
- Держите в памяти тот факт, что больной во время исследования лежит на спине. Поэтому, например, жидкость в плевральной полости не собирается в плевральных синусах, а «растекается» по нижней стенке плевральной полости;
- Будьте внимательны, проводя денситометрию: помните, что в срез может попадать не только интересующая Вас структура, особенно, если эта структура небольших размеров из-за эффектов частного объема. Всегда измеряйте плотность в нескольких разных областях органа; проводите денситометрию только на бесконтрастных сканах (или сравнивайте показатели денситометрии на при нативном и контрастном исследовании; в этом случае следите, чтобы показатели были взяты из одной области). Интерпретировать результаты денситометрии также следует с осторожностью: жидкость высокой плотности в плевральной полости может быть кровью, транссудатом, гноем, смесью крови и экссудата и т. д; повышение плотности ткани печени — следствием цирротических изменений, диффузной формы злокачественного образования, а может быть и следствием нарушения обмена веществ, например, в виде отложений меди при болезни Вильсона-Коновалова.
А потому — главное правило: оценивайте изменения комплексно. Отмечайте не только изменение плотности, но и форму, объем, структуру органа; положение, форму, распространенность, контуры и структуру найденного образования и паттерн контрастного накопления. Сопоставляйте обнаруженные изменения с данными анамнеза и лабораторных исследований пациента. И помните, что любой метод имеет ограничения.
Робот-хирург и роботы-манекены, у которых бьется сердце, скачет давление, а зрачки реагируют на свет, — это тренажеры в симуляционном центре в московской больнице им. Боткина. На них учатся спасать раненных в авариях, делать многочасовые операции и принимать роды. Корреспонденты ТАСС побывали в классах, похожих на площадки для съемок фильмов-катастроф или популярных ситкомов про врачей, чтобы узнать, как эти технологии меняют медицину.
Спасти рядового "Умника"
За дверью с вывеской "Медицина катастроф" находится комната, стилизованная под станцию метро "Арбатская", на которой, по сценарию, поезд сошел с рельсов. Вместо одной стены здесь покореженный вагон с разбитыми окнами и дверьми. Внутри застыли пассажиры с открытыми ртами, перекошенными от ужаса. Посреди платформы лежит манекен, на первый взгляд — обычная пластиковая кукла. У другой стены — стулья, где нервничают люди в белых халатах.
"Чтобы сделать искусственное дыхание — нужно запрокинуть голову пострадавшего", — объясняет им преподаватель Людмила Байчорова. Она садится на коленки перед манекеном, берет его за подбородок и укладывает голову в правильное положение. Под подбородком у него показывается дыра, в ней видны провода.
Это робот "Умник". Он дышит, у него бьется сердце. Но сейчас он не подает признаков жизни. У слушателей курса два дня, а точнее 18 часов, чтобы научиться реанимировать его максимально быстро. Они по очереди выходят в центр комнаты.
— Мужчина-мужчина, что с вами? — первая слушательница хлопает по щеке робота. Нащупывает пульс на шее. Считает до десяти. Просит, обращаясь в толпу: "Девушка, вызовите скорую помощь".
— Стоп. Сначала хорошо, но пока вы считали, люди прибежали и начали помогать. Что надо было сделать? — спрашивает Байчорова.
— Объявить, чтобы не подходили! — подсказывают из зала.
— Не забываем, — кивает преподаватель.
При таких происшествиях не бывает тишины, как в классе. Инженер, наблюдающий за группой, включает спецэффекты. Свет гаснет почти полностью, из динамиков кричат: "На помощь!" Слушательница делает массаж сердца, включает дефибриллятор, чтобы дать разряд, делает искусственное дыхание. На поясе "Умника" есть табло — световой индикатор: он отображает сердцебиение, дыхание. Спустя несколько секунд на индикаторе поднимается белый столбик — курсантке удалось восстановить дыхание "пациента".
"Еще у робота поднимается грудная клетка, когда все получилось. Все очень реалистично, — говорит Людмила Байчорова. — Мы здесь обучаем работающих медиков. Они, конечно, умеют оказывать неотложную помощь. Но они по работе не сталкиваются с медициной катастроф. Есть, допустим, слушатели из психиатрических клиник. Мы учим, чтобы при необходимости они не растерялись, а делали все правильно. Искусственное дыхание, например, — это не так просто. Если воздух пойдет не в легкие, а в желудок — у пациента будут осложнения. Нельзя паниковать".
Слушатели имеют дело с реальными медприборами. "Это настоящий дефибриллятор — кстати, продвинутый: он анализирует состояние пациента, подсказывает действия, — говорит преподаватель. — Такие приборы создавались, чтобы ими могли пользоваться обычные люди без медицинского образования. А медикам они упрощают жизнь. Технологии помогают как в обучении, так и в работе".
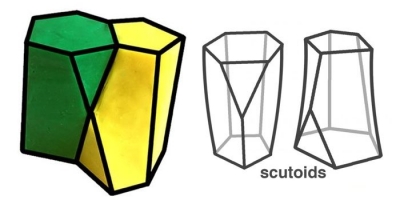
овая форма клеток, получившая название «скутоид», обеспечивает гибкость тканей эпителия при формировании органов. В перспективе результаты работы пригодятся при создании искусственных органов для трансплантации.
Ученые из Испании и США обнаружили ранее неизвестную геометрическую структуру, изучая особенности упаковки клеток эпителиальной ткани эмбрионов. Новую фигуру назвали скутоидом (scutoid). Исследование опубликовано в журнале Nature Communications.
Эпителий выстилает поверхность органов и внутренние полости тела, его клетки плотно прилегают друг к другу — межклеточного вещества между ними очень мало. Это качество принципиально важно для развития эмбриона: плотная ткань может легко изгибаться без повреждений по мере развития и роста органов. Авторы более ранних исследований считали, что клетки эпителия имеют форму призмы, «бутылки» или усеченной пирамиды.
Авторы новой работы смоделировали наиболее эффективные способы плотной упаковки клеток. Для этого использовали диаграмму Вороного — метод разбиения плоскости, при котором одна и та же точка будет ближайшей для всех точек, входящих в определенную ячейку. При моделировании ячейки диаграммы играли роль апикальной («наружной») поверхности клеток эпителия. Затем «семена» диаграммы — точки, вокруг которых строятся ячейки, — спроецировали на изнанку эпителия: эта часть клеток прилегает к базальной мембране, отделяющей эпителий от соединительной ткани.
Модель показала, что в плотной ткани должны присутствовать не только «призмы» и «бутылки», но и клетки более сложной формы. У одного из оснований такой фигуры насчитывалось шесть граней, у другого — пять, так как на боковой поверхности располагалась дополнительная треугольная грань. Фигура получила название «скутоид» в честь щитка насекомых (лат. scutellum), треугольной хитиновой пластины, хорошо заметной на спинке жуков и клопов.

Исследователи выяснили, что скутоиды действительно присутствуют в слюнных железах дрозофил и тканях зародышей рыб данио-рерио. Ученые считают, что эти структуры можно найти и в эпителии человека. Дальнейшее изучение скутоидов позволит усовершенствовать методы выращивания искусственных органов для пересадки.
Ранее исследователи из Нидерландов получили из стволовых клеток эмбрионы без яйцеклетки и сперматозоидов.
Американским микробиологам удалось заснять процесс генетической трансформации — поглощения бактерией чужой ДНК для приобретения новых признаков.
спространение новых признаков среди бактерий возможно не только «вертикально», от родителей к потомству, но и горизонтальным переносом — между клетками в популяции. Происходит это за счет генетической трансформации, поглощения клеткой случайных свободных цепочек ДНК из внешней среды и встраивания их в собственный геном. Так может передаваться и устойчивость к антибиотикам, что делает изучение этого механизма особенно актуальным.
Ученым из Университета Индианы впервые удалось увидеть этот процесс напрямую, с помощью микроскопа и нового метода наблюдений. Об этом Анкур Далия (Ankur Dalia) и его соавторы пишут в статье, опубликованной в журнале Nature Microbiology.
В каждый момент лишь незначительная часть популяции бактерий способна к «восприятию» чужой ДНК, однако эти так называемые компетентные клетки играют важнейшую роль в выживании. Их оболочки становятся более проницаемыми, а для поглощения ДНК используются пили — специализированные выросты на поверхности. Ученые стимулировали такое состояние компетентности у холерных вибрионов. Специализированный набор флуоресцентных красителей позволил визуализировать и клетки, и пили, и ДНК.

По словам авторов, пили действуют как миниатюрные — в десяток тысяч раз тоньше человеческого волоса — гарпуны, вытягиваясь из поры в клеточной стенке, захватывая ДНК и втягиваясь обратно. Да и поры настолько малы, что ДНК скручивается, чтобы протиснуться в отверстие. «Это как шитье ниткой, — объясняет Кортни Элисон (Courtney Ellison), одна из авторов работы. — Ширина отверстия во внешней оболочке почти равна спирали ДНК, сложенной вдвое. Если бы не пили, шансы на то, что ДНК, протолкнувшись в клетку, пройдет под нужным углом, практически нулевые».