Новости
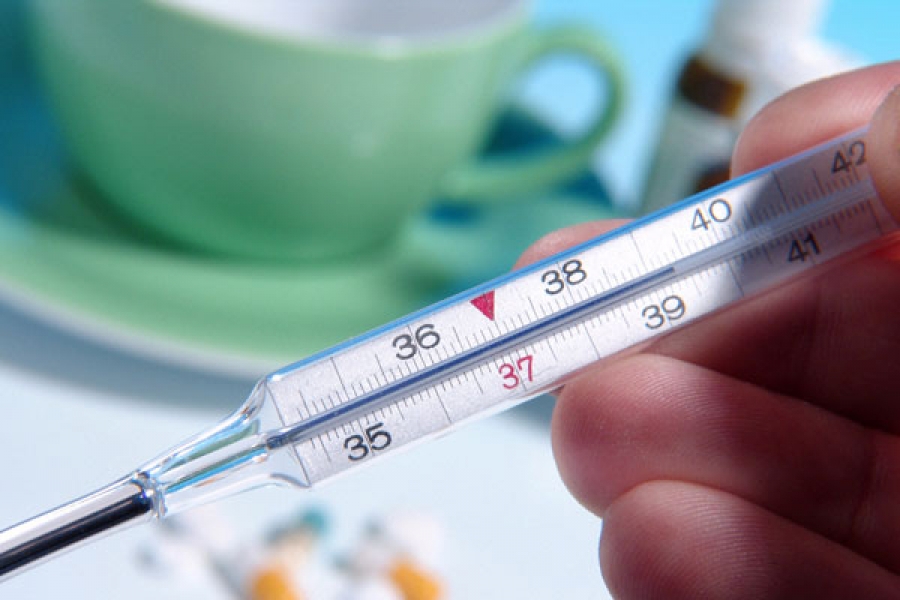
Министерством здравоохранения Российской Федерации в связи с возникновением случаев заболеваний российских граждан, отдыхающих на курортах Турецкой Республики, и поступившим письмом Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека о мерах в связи с ситуацией в Турции подготовлена памятка для населения по энтеровирусной инфекции:
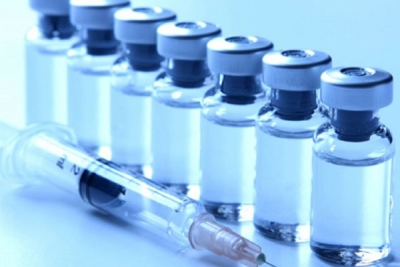
Поликлиники Луганска полностью обеспечены детскими вакцинами от гриппа. Об этом 14 августа рассказала главный врач городской детской больницы №2 Анна Доброхотова на совещании в Администрации города Луганска.
Низкокалорийная диета способна улучшить функционирование биологических часов в пожилом возрасте, препятствуя старению. Пока, впрочем, эти выводы в полной мере актуальны лишь в случае с грызунами.
Женщины-депутаты Народного Совета ЛНР прошли трехдневные курсы оказания первой помощи на базе Луганского республиканского центра экстренной медицинской помощи и медицины катастроф.
Когда в 1996г в Москву приехал легендарный Майкл Дебейки чтобы подстраховать наших врачей которые делали шунтирование сердца Ельцину он сказал журналистам что хотел бы поклониться Мастеру.
Ни один из журналистов не знал этой фамилии, тогда Дебейки повторил по слогам, пологая что его просто не понимают. Дебейки жалел что Мастер не врач, а биолог и не может продемонстрировать свою виртуозную технику операции на человеке.
Ученые исследовали вирусы герпеса и нашли антивирусный агент широкого спектра действия, который может быть эффективен даже против вируса Зика.
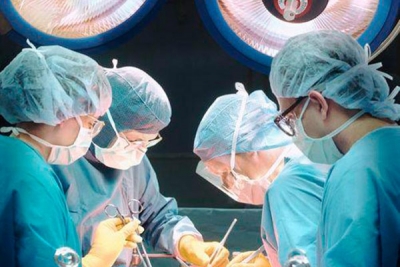
В Санкт-Петербурге, в Национальном медицинском исследовательском центре имени В.А. Алмазова Минздрава России, благодаря возможностям гибридной операционной, осуществлено уникальное оперативное вмешательство при артериовенозной мальформации (АВМ) головного мозга